In der faszinierenden Welt der Chemie stoßen wir immer wieder auf Begriffe, die uns neugierig machen. Was ist ein Ampholyt und warum ist er so wichtig für viele chemische Prozesse? Ampholyte sind Verbindungen, die sowohl als Säure als auch als Base fungieren können. Sie spielen eine zentrale Rolle in biologischen Systemen und industriellen Anwendungen.
Was Ist Ein Ampholyt?
Ampholyte sind Substanzen, die sowohl als Säure als auch als Base wirken können. Dieses duale Verhalten ermöglicht ihnen, in verschiedenen chemischen Reaktionen flexibel zu agieren. Besonders wichtig ist, dass sie in biologischen Systemen und industriellen Anwendungen eine zentrale Rolle spielen.
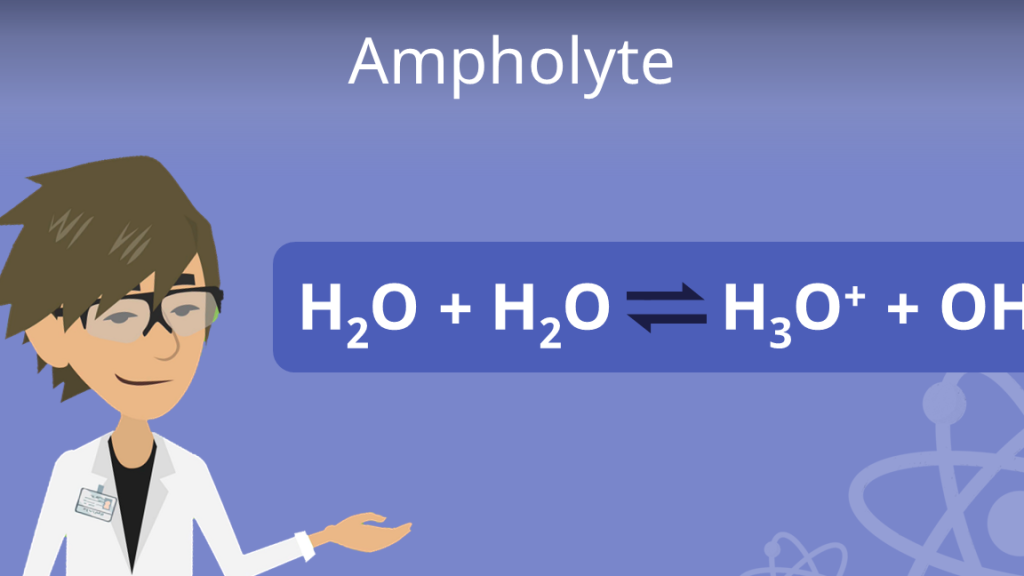
Ampholyte stehen im Gleichgewicht, je nach dem pH-Wert der Umgebung:
Ein häufiges Beispiel für einen Ampholyten ist Wasser. Es kann sowohl Protonen aufnehmen als auch abgeben, was es zu einem ausgezeichneten Lösungsmittel macht.
Die Funktion von Ampholyten in biologischen Systemen hat weitreichende Konsequenzen. Sie helfen bei der Regulierung des pH-Wertes in Zellen und Körperflüssigkeiten. Folgende Beispiele verdeutlichen ihre Bedeutung:
In industriellen Anwendungen finden wir Ampholyte oft in der Textil- und Lebensmittelproduktion. Ihre Fähigkeit, sowohl Säuren als auch Basen zu neutralisieren, ist besonders vorteilhaft.
Eigenschaften Von Ampholyten
Ampholyte zeigen vielseitige Eigenschaften, die sie sowohl in biologischen als auch industriellen Kontexten bedeutend machen. Wir betrachten hier die wichtigsten Eigenschaften im Detail.
Säure-Base-Verhalten
Ampholyte besitzen die Fähigkeit, sowohl Protonen abzugeben als auch aufzunehmen, was zu ihrem Verhalten als Säure oder Base führt. Wichtig ist, dass dieses Verhalten vom pH-Wert der Umgebung abhängt. Wir listen die Hauptmerkmale auf:
Solche Eigenschaften erzeugen ein Gleichgewicht, das entscheidend für viele chemische und biologische Prozesse ist.
Lösungen Und Ionenstärke
Die Eigenschaften von Ampholyten in Lösungen variieren je nach Ionenstärke, was ihre Wechselwirkungen beeinflusst. Wir betrachten wichtige Aspekte:
Die Fähigkeit, sich an unterschiedliche Umgebungen anzupassen, macht Ampholyte vielseitig und funktional in zahlreichen Anwendungen.
Anwendungen Von Ampholyten
Ampholyte finden in verschiedenen Bereichen bedeutende Anwendungen. Ihre Fähigkeit, sowohl als Säure als auch als Base zu wirken, macht sie in vielen wissenschaftlichen und industriellen Prozessen unverzichtbar.
Biochemie
In der Biochemie desempeñen Ampholyte eine zentrale Rolle. Sie sind essenziell für die Regulierung des pH-Wertes in biologischen Systemen. Weitere wichtige Anwendungen sind:
Diese Eigenschaften unterstützen die Funktion von Enzymen und die Durchführung biochemischer Reaktionen.
Chemische Analysen
Ampholyte sind auch entscheidend für Chemische Analysen. Ihre Fähigkeit, multiple Ionisierungsstufen anzunehmen, erlaubt präzise Messungen in verschiedenen chemischen Umgebungen. Hier einige ihrer Funktionen:
Diese Anwendungen verdeutlichen die Vielseitigkeit und Wichtigkeit von Ampholyten in der Wissenschaft.
Beispiele Für Ampholyte
Ampholyte finden sich in vielen chemischen und biologischen Kontexten. Ihre Fähigkeit, sowohl als Protonenakzeptoren als auch als Protonenspender zu fungieren, macht sie besonders vielseitig. Hier sind einige bedeutende Beispiele:
- Wasser: Wasser wirkt als Ampholyte, da es sowohl Protonen aufnehmen als auch abgeben kann, was es zu einem hervorragenden Lösungsmittel macht.
- Aminosäuren: Sie wirken als Ampholyte, weil sie sowohl saure als auch basische Gruppen enthalten. Dies ermöglicht die Anpassung ihrer Eigenschaften an verschiedene pH-Werte.
- Bikarbonat: Dieses Molekül spielt eine wichtige Rolle als Blutpuffer und kann als Säure oder Base agieren, um den pH-Wert im Blut stabil zu halten.
- Proteine: Sie konfigurieren sich in Abhängigkeit vom pH-Wert der Umgebung und zeigen Ampholyteigenschaften, was ihre biologischen Funktionen unterstützt.
- Acetat: Als Teil von Pufferlösungen stabilisiert Acetat den pH-Wert und nutzt seine Ampholyteigenschaften zur Regulierung chemischer Reaktionen.
Die Beispiele verdeutlichen die bedeutende Rolle von Ampholyten in lebenden Organismen und industriellen Prozessen. Jede dieser Verbindungen zeigt, wie wichtig die Fähigkeit zur Einnahme unterschiedlicher Protonen in verschiedenen Umgebungen ist.
Fazit
Ampholyte sind unverzichtbar in der Chemie und Biochemie. Ihre Fähigkeit sowohl als Säure als auch als Base zu agieren macht sie zu wichtigen Akteuren in vielen Prozessen. Wir erkennen, dass sie nicht nur in biologischen Systemen eine zentrale Rolle spielen, sondern auch in industriellen Anwendungen von großer Bedeutung sind.
Die vielseitigen Eigenschaften von Ampholyten ermöglichen es uns, präzise chemische Analysen durchzuführen und pH-Werte effektiv zu regulieren. Ob in der Textilindustrie oder in der Lebensmittelproduktion ihre Anpassungsfähigkeit zeigt sich in zahlreichen Anwendungen.
Wir sollten die Bedeutung von Ampholyten weiterhin erforschen und ihre Rolle in der Wissenschaft und Industrie wertschätzen.