Die Atombindung ist ein zentrales Konzept in der Chemie, das unser Verständnis von Molekülen und deren Eigenschaften prägt. In diesem Artikel werden wir die Grundlagen der Atombindung erkunden und einige anschauliche Beispiele betrachten. Durch das Verständnis dieser Bindungen können wir die Wechselwirkungen zwischen Atomen besser nachvollziehen.
Wir zeigen Ihnen, wie Atome durch Elektronenpaare miteinander verbunden sind und welche Rolle diese Bindungen in alltäglichen Substanzen spielen. Die Atombindung ist nicht nur für Chemiker wichtig sondern auch für alle, die sich mit Naturwissenschaften beschäftigen. Welche Fragen zur Atombindung beschäftigen Sie? Lassen Sie uns gemeinsam tiefere Einblicke in diese faszinierende Thematik gewinnen!
Atombindung: Definition und Bedeutung in der Chemie
Die Atombindung, auch als kovalente Bindung bekannt, ist ein fundamentaler Aspekt der Chemie, der die Wechselwirkungen zwischen Atomen beschreibt. Bei dieser Art der Bindung teilen sich zwei Atome Elektronenpaare, um eine stabilere elektronische Konfiguration zu erreichen. Diese Stabilität führt dazu, dass Moleküle gebildet werden, die für alle chemischen Reaktionen und die Struktur von Substanzen von zentraler Bedeutung sind.
In der Chemie spielt die Atombindung eine entscheidende Rolle, da sie nicht nur die Eigenschaften von Stoffen beeinflusst, sondern auch deren Verhalten in chemischen Reaktionen bestimmt. Durch das Verständnis der Atombindungen können wir Vorhersagen über die Reaktivität und Stabilität verschiedener chemischer Verbindungen treffen.
Die Bedeutung der Atombindung
Die Bedeutung der Atombindung lässt sich in mehreren Punkten zusammenfassen:
- Stabilität: Die Bildung einer Atombindung ermöglicht es den beteiligten Atomen, energetisch günstige Zustände zu erreichen.
- Vielfalt an Molekülen: Durch verschiedene Kombinationen von Atomtypen entstehen unzählige Moleküle mit unterschiedlichen Eigenschaften.
- Einfluss auf physikalische Eigenschaften: Die Art und Weise, wie Atome miteinander verbunden sind, beeinflusst direkt Eigenschaften wie Siedepunkte, Löslichkeit und Härte.
Zusammengefasst ist die Atombindung ein zentrales Konzept in der Chemie. Sie erklärt nicht nur das Verhalten von Materie auf atomarer Ebene sondern bildet auch die Grundlage für viele wissenschaftliche Disziplinen wie Biochemie und Materialwissenschaften.
Arten der Atombindung: Kovalente und ionische Bindungen
Die Atombindung kann in zwei Hauptarten unterteilt werden: die kovalente Bindung und die ionische Bindung. Beide Typen sind entscheidend für das Verständnis der chemischen Struktur und Eigenschaften von Molekülen. Während bei der kovalenten Bindung Elektronenpaare zwischen Atomen geteilt werden, findet bei der ionischen Bindung eine Übertragung von Elektronen statt, was zu einer Anziehung zwischen positiv und negativ geladenen Ionen führt.
Kovalente Bindungen
Kovalente Bindungen entstehen, wenn zwei oder mehr Atome ihre Valenzelektronen teilen, um eine stabilere elektronische Konfiguration zu erreichen. Dieser Teilungsprozess ermöglicht es den beteiligten Atomen, eine energetisch günstigere Zustand zu erreichen. Kovalente Bindungen können einfach (ein Paar geteilter Elektronen), doppelt (zwei Paare) oder sogar dreifach (drei Paare) sein. Die Stärke dieser Bindungen hängt von der Anzahl der geteilten Elektronenpaare ab.
Ein Beispiel für eine kovalente Verbindung ist Wasser (H₂O), wo jedes Wasserstoffatom ein Elektron mit dem Sauerstoffatom teilt. Diese Art der Atombindung spielt nicht nur in anorganischen Verbindungen eine Rolle, sondern auch in organischen Molekülen wie Kohlenhydraten und Proteinen.
Ionische Bindungen
Im Gegensatz dazu erfolgt bei ionischen Bindungen die Übertragung von Elektronen von einem Atom auf ein anderes. Dies geschieht häufig zwischen einem Metall und einem Nichtmetall. Das Metall gibt seine Valenzelektronen ab und wird dabei positiv geladen, während das Nichtmetall diese Elektronen aufnimmt und negativ geladen wird. Die entstehenden Ionen ziehen sich aufgrund ihrer gegensätzlichen Ladungen an, was zur Bildung eines stabilen ionischen Kristalls führt.
Ein klassisches Beispiel für ionische Bindungen ist Natriumchlorid (NaCl). Hierbei verliert Natrium ein Elektron und wird zum Na⁺-Ion, während Chlor ein Electron aufnimmt und zum Cl⁻-Ion wird. Diese starke elektrostatische Anziehung zwischen den Ionen sorgt dafür, dass sich Salzkristalle bilden.
Beide Arten der Atombindung sind grundlegend für die Vielfalt chemischer Verbindungen in unserer Welt und beeinflussen maßgeblich deren physikalische Eigenschaften sowie Reaktivität in chemischen Reaktionen.
Eigenschaften von Molekülen mit Atombindung
Moleküle, die durch Atombindung entstehen, weisen eine Vielzahl von Eigenschaften auf, die sie von anderen chemischen Verbindungen unterscheiden. Diese Eigenschaften sind entscheidend für das Verständnis ihrer Reaktivität und Anwendungen in der Chemie. Zu den wichtigsten Merkmalen zählen die Polarität, der Schmelz- und Siedepunkt sowie die Löslichkeit in verschiedenen Lösungsmitteln.
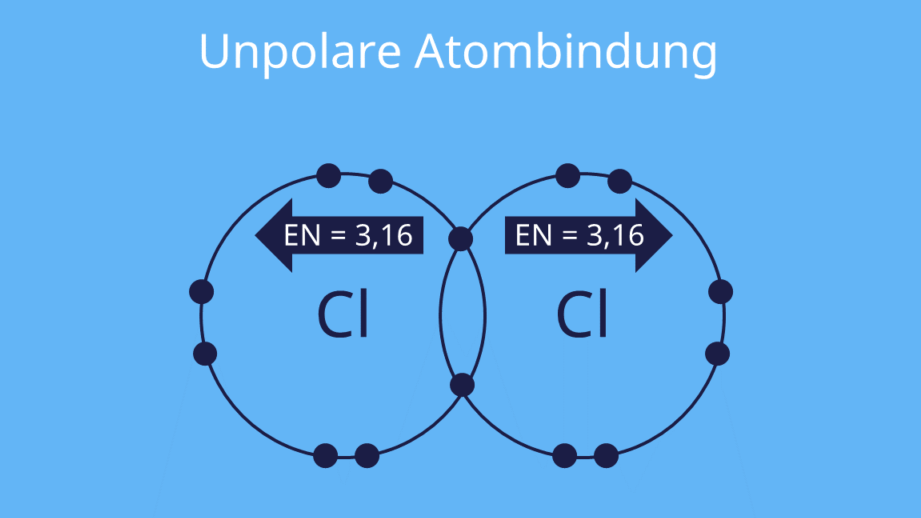
Ein zentrales Konzept ist die Polarität von Molekülen. Moleküle mit Atombindung können polar oder unpolar sein, abhängig von der Elektronegativitätsdifferenz zwischen den gebundenen Atomen. Bei polaren Molekülen verteilt sich die elektrische Ladung asymmetrisch, was zu einer positiven und einer negativen Seite führt. Im Gegensatz dazu haben unpolare Moleküle eine symmetrische Ladungsverteilung.
Die Schmelz- und Siedepunkte solcher Verbindungen variieren erheblich. Kovalente Verbindungen haben im Allgemeinen niedrigere Schmelz- und Siedepunkte als ionische Verbindungen aufgrund der schwächeren intermolekularen Kräfte. Beispielsweise hat Wasser (H₂O) einen relativ hohen Siedepunkt verglichen mit anderen kleinen Molekülen wie Methan (CH₄), was auf Wasserstoffbrücken zurückzuführen ist, die zwischen Wassermolekülen wirken.
Die Löslichkeit von molekularen Verbindungen hängt ebenfalls stark von ihrer Polarität ab. Polare Moleküle lösen sich gut in polaren Lösungsmitteln wie Wasser, während unpolare Moleküle besser in unpolaren Lösungsmitteln wie Benzin löslich sind. Dies folgt dem Prinzip „Ähnliches löst Ähnliches“, das besagt, dass Stoffe mit ähnlichen chemischen Eigenschaften sich gegenseitig lösen können.
| Eigenschaft | Beschreibung |
|---|---|
| Polarität | Asymmetrische Ladungsverteilung; kann polar oder unpolar sein. |
| Schmelzpunkt | Niedriger bei kovalenten Bindungen im Vergleich zu ionischen. |
| Siedepunkt | Variiert je nach intermolekularer Kraft; höher bei starken Wechselwirkungen. |
| Löslichkeit | Polares löst sich gut in polaren Lösungsmitteln; unpolares in unpolaren. |
Diese Eigenschaften machen klar, dass Atombindungen nicht nur für die Struktur eines Moleküls entscheidend sind, sondern auch dessen Verhalten unter verschiedenen Bedingungen maßgeblich beeinflussen. Daher spielen sie eine zentrale Rolle beim Verständnis chemischer Reaktionen und der Entwicklung neuer Materialien in der Chemie.
Beispiele für Atombindungen in alltäglichen Substanzen
Atombindungen sind in vielen alltäglichen Substanzen zu finden, die wir täglich nutzen oder konsumieren. Diese Bindungen sind entscheidend für die chemischen Eigenschaften und das Verhalten dieser Stoffe. Zu den bekanntesten Beispielen gehören Wasser, Kohlenstoffdioxid und organische Verbindungen wie Zucker und Fette.
Wasser (H₂O)
Wasser ist eines der wichtigsten Moleküle auf der Erde und besteht aus zwei Wasserstoffatomen, die durch Atombindung mit einem Sauerstoffatom verbunden sind. Diese kovalente Bindung verleiht dem Wasser seine einzigartigen Eigenschaften, einschließlich hoher Polarität und Fähigkeit zur Bildung von Wasserstoffbrücken. Diese Brücken sind verantwortlich für viele physikalische Eigenschaften des Wassers, wie z.B. seinen hohen Siedepunkt im Vergleich zu anderen Molekülen ähnlicher Größe.
Kohlenstoffdioxid (CO₂)
Kohlenstoffdioxid ist ein weiteres Beispiel für eine Verbindung mit Atombindungen. Es besteht aus einem Kohlenstoffatom, das doppelt mit zwei Sauerstoffatomen verbunden ist. Die lineare Struktur des CO₂-Moleküls führt zu einer unpolaren Natur, weshalb es in Wasser nur begrenzt löslich ist. Dieses Gas spielt eine wesentliche Rolle im globalen Kohlenstoffkreislauf sowie in biologischen Prozessen wie der Photosynthese.
Zucker (C₁₂H₂₂O₁₁)
Zucker ist ein Beispiel für komplexere organische Verbindungen, die zahlreiche Atombindungen enthalten. Saccharose, der häufigste Haushaltszucker, setzt sich aus Glukose- und Fruktosemolekülen zusammen, die durch glykosidische Bindungen verknüpft sind. Diese spezifische Art der Atombindung beeinflusst nicht nur den Geschmack von Zucker sondern auch seine Löslichkeit in Wasser sowie andere chemische Reaktionen während des Kochens oder Backens.
| Substanz | Formel | Bedeutung |
|---|---|---|
| Wasser | H₂O | Lösungsmittel für viele chemische Reaktionen; lebenswichtig für alle Organismen. |
| Kohlenstoffdioxid | CO₂ | Beteiligt an der Photosynthese; Treibhausgas. |
| Zucker | C₁₂H₂₂O₁₁ | Energiequelle; wichtig für den menschlichen Geschmackssinn. |
Diese Beispiele verdeutlichen die zentrale Rolle von Atombindungen in alltäglichen Substanzen und deren Einfluss auf unsere Umwelt sowie unser tägliches Leben. Das Verständnis dieser Bindungen hilft uns nicht nur bei der Bewertung chemischer Reaktionen sondern auch bei der Entwicklung neuer Materialien und Anwendungen in verschiedenen Bereichen wie Medizin oder Ernährung.
Die Rolle der Elektronegativität bei chemischen Bindungen
Die Elektronegativität spielt eine entscheidende Rolle bei der Bildung von Atombindungen. Sie beschreibt die Fähigkeit eines Atoms, Elektronen in einer chemischen Bindung anzuziehen. Diese Eigenschaft variiert zwischen den Elementen und beeinflusst maßgeblich, wie Atome miteinander interagieren, um stabile Moleküle zu bilden. Der Unterschied in der Elektronegativität zwischen zwei Atomen bestimmt nicht nur die Art der Bindung, sondern auch die physikalischen und chemischen Eigenschaften des resultierenden Moleküls.
Ein großer Unterschied in der Elektronegativität führt oft zu ionischen Bindungen, während ein kleinerer Unterschied kovalente Bindungen zur Folge hat. Aber nicht nur das; auch innerhalb kovalenter Bindungen kann es Unterschiede geben, die zu polarisierten Molekülen führen. In einem polaren Molekül ziehen beispielsweise die elektronegativeren Atome stärker an den gemeinsamen Elektronenpaaren als ihre weniger elektronegativen Partner.
Die Bedeutung von Pauling-Skala
Um die Elektronegativität quantifizierbar zu machen, nutzen Chemiker häufig die Pauling-Skala. Diese Skala ordnet jedem Element einen Wert zu, der seine Fähigkeit zur Anziehung von Elektronen widerspiegelt:
- Fluor (F): 4.0 (höchste Elektronegativität)
- Sauerstoff (O): 3.5
- Stickstoff (N): 3.0
- Kohlenstoff (C): 2.5
- Wasserstoff (H): 2.1
Diese Werte ermöglichen es uns, vorherzusagen, welche Art von Bindung zwischen zwei bestimmten Elementen bestehen wird.
Einfluss auf molekulare Eigenschaften
Die unterschiedlichen Arten von Atombindungen beeinflussen direkt verschiedene Eigenschaften von Molekülen:
- Polarität: Polare Moleküle haben aufgrund ihrer ungleichen Ladungsverteilung einzigartige Eigenschaften wie höhere Siedepunkte.
- Reaktivität: Die Reaktivität eines Stoffes kann durch seine elektronegativen Eigenschaften bestimmt werden; Elemente mit hoher Elektronegativität neigen dazu, leicht mit anderen Elementen zu reagieren.
Insgesamt ist das Verständnis der Rolle der Elektronegativität unerlässlich für unser Wissen über chemische Reaktionen und die Gestaltung neuer Verbindungen in Bereichen wie Materialwissenschaften und Biochemie.