Das chemische Gleichgewicht ist ein faszinierendes Konzept, das in der Chemie eine zentrale Rolle spielt. Es beschreibt den Zustand, in dem die Geschwindigkeit der Hin- und Rückreaktion gleich ist und somit die Konzentrationen der Reaktanten und Produkte konstant bleiben. In unserem Artikel werden wir die Grundlagen des chemischen Gleichgewichts beleuchten und seine bedeutende Rolle in verschiedenen chemischen Prozessen erklären.
Wir alle haben uns schon gefragt, wie chemische Reaktionen ablaufen und was passiert, wenn sie sich im Gleichgewicht befinden. Dieses Wissen ist nicht nur für Chemiker von Bedeutung sondern auch für viele Bereiche unseres täglichen Lebens wie Medizin Umweltwissenschaften oder Ingenieurwesen. Wir werden untersuchen warum das Verständnis des chemischen Gleichgewichts entscheidend für die Entwicklung neuer Technologien und Medikamente ist.
Wie beeinflusst das chemische Gleichgewicht unsere Welt? Sind Sie bereit zu entdecken wie dieses Prinzip unser Leben prägt? Lassen Sie uns gemeinsam in diese spannende Materie eintauchen!
Chemisches Gleichgewicht: Definition und Grundlagen
Das chemische Gleichgewicht ist ein fundamentaler Zustand in der Chemie, der beschreibt, wie sich die Konzentrationen von Reaktanten und Produkten in einer reversiblen chemischen Reaktion über die Zeit stabilisieren. In diesem Zustand sind die Geschwindigkeiten der Hin- und Rückreaktionen gleich, was bedeutet, dass keine Nettoänderung in den Konzentrationen auftritt. Dies führt zu einem dynamischen Gleichgewicht, bei dem molekulare Veränderungen kontinuierlich stattfinden, jedoch keine sichtbaren Veränderungen im Makroskopischen auftreten.
Im chemischen Gleichgewicht spielt die Reaktionsgeschwindigkeit eine entscheidende Rolle. Diese Geschwindigkeit wird durch verschiedene Faktoren beeinflusst, darunter Temperatur, Druck und Konzentration der Reaktanten sowie Produkte. Ein tiefes Verständnis dieser Konzepte ermöglicht es uns, gezielt Eingriffe vorzunehmen und das Gleichgewicht zu verschieben – ein Prinzip, das als Le Châtelier-Prinzip bekannt ist.
Grundlegende Konzepte des chemischen Gleichgewichts
Um das Konzept des chemischen Gleichgewichts besser zu verstehen, sollten wir einige grundlegende Begriffe definieren:
- Reversible Reaktionen: Chemische Reaktionen können oft in beide Richtungen ablaufen (Hin- und Rückreaktion).
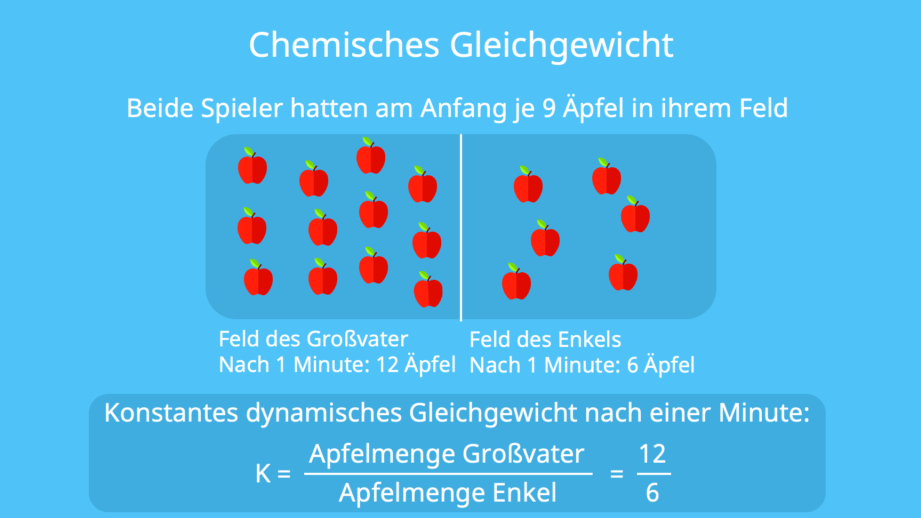
- Konzentrationsausdrücke: Das Verhältnis von Produktkonzentrationen zur Reaktantenkonzentration wird durch die Gleichgewichtskonstante K beschrieben.
| Gleichung | Beschreibung |
|---|---|
| K = [Produkte]/[Reaktanten] | Definiert das Verhältnis von Produkt- zu Reaktantenkonzentrationen im Gleichgewicht. |
Durch diese Definitionen können wir erkennen, dass das chemische Gleichgewicht nicht statisch ist; vielmehr handelt es sich um einen dynamischen Prozess. Die Fähigkeit eines Systems, auf äußere Einflüsse zu reagieren und neue Bedingungen anzunehmen oder zurückzukehren zum ursprünglichen Zustand ist entscheidend für viele industrielle Anwendungen sowie für unsere allgemeine Wissensbasis in der Chemie.
Zusammenfassend lässt sich sagen, dass das chemische Gleichgewicht ein komplexes Zusammenspiel zwischen verschiedenen Faktoren darstellt und unser Verständnis davon essenziell für zahlreiche wissenschaftliche Fortschritte ist.
Die Rolle der Temperatur im chemischen Gleichgewicht
Die Temperatur hat einen entscheidenden Einfluss auf das chemische Gleichgewicht, indem sie die Reaktionsgeschwindigkeit und die Position des Gleichgewichts beeinflusst. Ein Anstieg der Temperatur führt in der Regel dazu, dass sich die kinetischen Energien der Moleküle erhöhen, was zu schnelleren Reaktionen führt. Dies kann sowohl die Hinreaktion als auch die Rückreaktion betreffen. Um den Effekt der Temperatur auf das chemische Gleichgewicht besser zu verstehen, ist es wichtig, das Le Châtelier-Prinzip anzuwenden.
Gemäß dem Le Châtelier-Prinzip verschiebt sich das Gleichgewicht einer Reaktion in Richtung der Seite, die Wärme absorbiert, wenn eine Temperaturerhöhung erfolgt. Bei exothermen Reaktionen wird also oft beobachtet, dass ein Anstieg der Temperatur zu einer Abnahme der Produktkonzentration führt. Im Gegensatz dazu fördern endotherme Reaktionen eine Zunahme von Produkten bei höherer Temperatur.
Einfluss auf exotherme und endotherme Reaktionen
Um diese Konzepte weiter zu verdeutlichen, betrachten wir einige Beispiele:
- Exotherme Reaktionen: Diese setzen Wärme frei (z.B. Verbrennung). Ein Beispiel ist die Synthese von Ammoniak aus Stickstoff und Wasserstoff:
[
N_2(g) + 3 H_2(g) rightleftharpoons 2 NH_3(g) + text{Wärme}
]
- Endotherme Reaktionen: Diese benötigen Wärme (z.B. Photosynthese). Ein Beispiel wäre:
[
CO_2(g) + H_2O(l) + text{Wärme} rightleftharpoons C_6H_{12}O_6(aq)
]
Zusammenfassung der temperaturabhängigen Effekte
| Art der Reaktion | Wirkung einer Temperaturerhöhung |
|---|---|
| Exotherm | Verschiebung des Gleichgewichts nach links (weniger Produkte) |
| Endotherm | Verschiebung des Gleichgewichts nach rechts (mehr Produkte) |
Durch das Verständnis dieser Zusammenhänge können wir gezielt Temperatureffekte nutzen, um gewünschte Produktkonzentrationen in industriellen Prozessen zu optimieren und somit effizientere Produktionsmethoden im Rahmen des chemischen Gleichgewichts zu entwickeln.
Einfluss von Druck und Konzentration auf das Gleichgewicht
Die Veränderung des Drucks und der Konzentration hat ebenfalls einen entscheidenden Einfluss auf das chemische Gleichgewicht. Diese beiden Faktoren wirken direkt auf die Position des Gleichgewichts und können, ähnlich wie die Temperatur, dazu verwendet werden, gewünschte Produktkonzentrationen in Reaktionen zu steuern. Laut dem Le Châtelier-Prinzip wird das Gleichgewicht einer Reaktion so verschoben, dass es den Veränderungen standhält.
Wenn wir über den Druck sprechen, ist es wichtig zu beachten, dass dieser hauptsächlich bei gasförmigen Reaktionen von Bedeutung ist. Eine Erhöhung des Drucks führt dazu, dass sich das Gleichgewicht in Richtung der Seite mit weniger Molekülen verschiebt. Umgekehrt bewirkt eine Drucksenkung eine Verschiebung in Richtung der Seite mit mehr Molekülen. Dies können wir anhand eines klassischen Beispiels verdeutlichen:
- Reaktion mit weniger Molekülen:
[
N_2(g) + 3 H_2(g) rightleftharpoons 2 NH_3(g)
]
Hier führt eine Druckerhöhung zur Bildung von Ammoniak (NH₃).
- Reaktion mit mehr Molekülen:
[
CO(g) + H_2O(g) rightleftharpoons CO_2(g) + H_2(g)
]
In diesem Fall würde eine Druckerhöhung die Rückreaktion begünstigen.
Im Hinblick auf die Konzentration gilt Folgendes: Eine Erhöhung der Konzentration eines Reaktanten verschiebt das Gleichgewicht in Richtung der Produkte, während eine Verringerung zu einer Verschiebung in Richtung der Edukte führt. Dies ermöglicht uns gezielte Anpassungen im Labor oder industriellen Prozessen vorzunehmen.
Beispiele für den Einfluss von Druck und Konzentration
Um diese Konzepte anschaulicher zu machen, betrachten wir einige Beispiele:
- Druck: Bei der Synthese von Ammoniak führen hohe Drücke zur Bevorzugung der Bildung von NH₃.
- Konzentration: Wenn wir Wasserstoffgas (H₂) erhöhen, wird die Produktion von Ammoniak gefördert.
| Faktor | Einfluss auf das Gleichgewicht |
|---|---|
| Druck erhöhen | Verschiebung zum Bereich mit weniger Gas-Molekülen |
| Konzentration erhöhen (Edukt) | Verschiebung nach rechts (Produkte) |
| Konzentration reduzieren (Produkt) | Verschiebung nach links (Edukte) |
Durch ein tiefes Verständnis dieser Einflüsse können wir optimale Bedingungen schaffen, um chemische Prozesse effizienter zu gestalten und somit erfolgreichere industrielle Anwendungen des chemischen Gleichgewichts zu realisieren.
Anwendungen des chemischen Gleichgewichts in der Industrie
Die Anwendung des chemischen Gleichgewichts in der Industrie ist von großer Bedeutung, da sie uns ermöglicht, Produktionsprozesse zu optimieren und die Effizienz zu steigern. In verschiedenen Bereichen, wie der chemischen Synthese oder der petrochemischen Industrie, spielt das Verständnis des chemischen Gleichgewichts eine zentrale Rolle. Durch gezielte Steuerung von Temperatur, Druck und Konzentration können wir die Ausbeute an gewünschten Produkten maximieren und gleichzeitig die Kosten minimieren.
### Chemische Synthese
Ein herausragendes Beispiel für die Anwendung des chemischen Gleichgewichts in der Industrie ist die Ammoniaksynthese. Hierbei wird Stickstoffgas (N₂) mit Wasserstoffgas (H₂) unter hohem Druck und bei moderaten Temperaturen kombiniert:
[
N_2(g) + 3 H_2(g) rightleftharpoons 2 NH_3(g)
]
Durch Erhöhung des Drucks verschiebt sich das Gleichgewicht nach Le Châtelier zugunsten der Produktbildung, was zur Herstellung von Ammoniak führt. Diese Reaktion ist nicht nur energieeffizient, sondern auch entscheidend für die Düngemittelproduktion.
### Petrochemische Prozesse
In der petrochemischen Industrie finden zahlreiche Reaktionen statt, bei denen das chemische Gleichgewicht eine wesentliche Rolle spielt. Beispielsweise wird bei der katalytischen Reformierung von n-Butan (C₄H₁₀) Benzin durch folgende Reaktion produziert:
[
C_4H_{10}(g) rightleftharpoons C_6H_{14}(g)
]
Hierbei kann durch Variation von Druck und Temperatur ebenfalls eine Verschiebung des Gleichgewichts erreicht werden, um den gewünschten Kraftstoffanteil zu erhöhen.
| Prozess | Reaktion | Einflussfaktoren |
|---|---|---|
| Ammoniaksynthese | N₂ + 3 H₂ ⇌ 2 NH₃ | Druck erhöhen; Temperatur senken |
| Katalytische Reformierung | C₄H₁₀ ⇌ C₆H₁₄ | Druck und Temperatur optimal einstellen |
### Weitere Anwendungen
Zusätzlich finden wir Anwendungen des chemischen Gleichgewichts in anderen Industrien wie der Lebensmittelverarbeitung oder der Pharmaindustrie. Im Bereich der Fermentation beispielsweise nutzen wir das Gleichgewicht zwischen Edukten und Produkten zur Maximierung unserer Erträge an Ethanol oder anderen Bioprodukten.
Indem wir diese Prinzipien verstehen und anwenden, können wir nicht nur unsere Produktionsprozesse verbessern, sondern auch einen nachhaltigen Beitrag zur Ressourcenschonung leisten.
Beispiele für chemische Reaktionen im Gleichgewicht
Das Verständnis von chemischen Reaktionen im Gleichgewicht ist entscheidend für viele Prozesse in der Industrie und Natur. In dieser Sektion werden wir einige prägnante Beispiele untersuchen, die das Konzept des chemischen Gleichgewichts veranschaulichen und dessen praktische Anwendung verdeutlichen.
Beispiel 1: Die Esterbildung
Ein klassisches Beispiel für eine chemische Reaktion im Gleichgewicht ist die Bildung von Estern aus Carbonsäuren und Alkoholen. Diese Reaktion kann wie folgt dargestellt werden:
[
RCOOH + R’OH rightleftharpoons RCOOR‘ + H_2O
]
In diesem Prozess reagieren eine Carbonsäure (RCOOH) und ein Alkohol (R’OH), um einen Ester (RCOOR‘) und Wasser zu bilden. Die Bedingungen wie Temperatur und Konzentration beeinflussen das Gleichgewicht, sodass durch gezielte Anpassungen die Ausbeute an Estern maximiert werden kann.
Beispiel 2: Die Haber-Bosch-Reaktion
Ein weiteres bedeutendes Beispiel ist die Haber-Bosch-Reaktion zur Ammoniakproduktion, welche bereits erwähnt wurde. Hierbei wird Stickstoffgas (N₂) mit Wasserstoffgas (H₂) kombiniert:
[
N_2(g) + 3 H_2(g) rightleftharpoons 2 NH_3(g)
]
Durch den Einsatz hoher Drücke sowie moderater Temperaturen können wir das Gleichgewicht zugunsten der Produktbildung verschieben, was nicht nur ökonomisch vorteilhaft ist, sondern auch essentiell für die Düngemittelherstellung.
Tabelle der Beispiele
| Reaktion | Gleichung | Einflussfaktoren |
|---|---|---|
| Esterbildung | RCOOH + R’OH ⇌ RCOOR‘ + H₂O | Konzentration erhöhen; Temperatur variieren |
| Ammoniaksynthese | N₂ + 3 H₂ ⇌ 2 NH₃ | Druck erhöhen; Temperatur senken |
Diese Beispiele zeigen deutlich, dass das chemische Gleichgewicht nicht nur ein theoretisches Konzept ist, sondern aktiv in industriellen Prozessen eingesetzt wird. Durch das gezielte Steuern der Einflussfaktoren können wir unsere Produktionsziele erreichen und dabei effizient arbeiten.