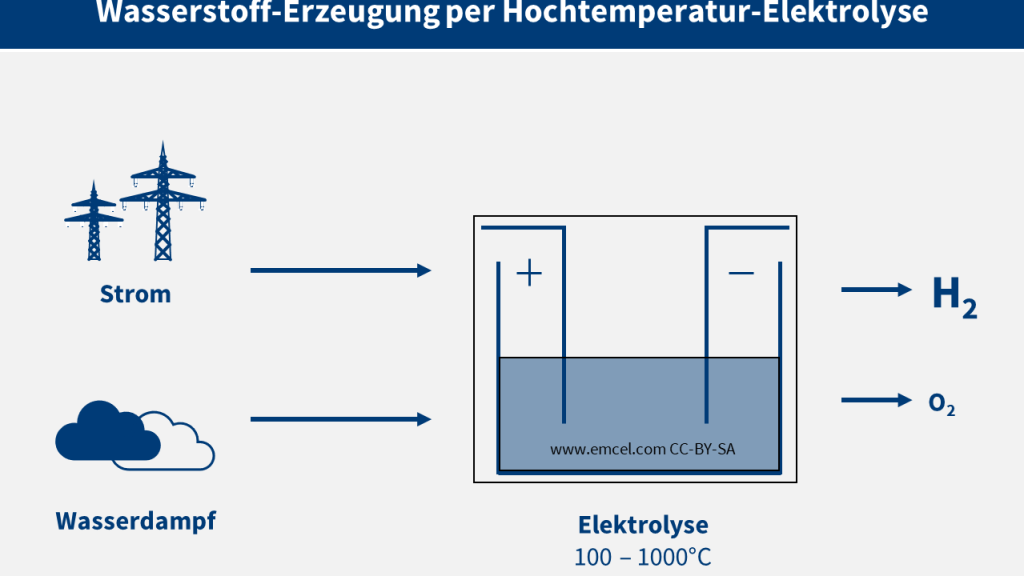
Hast du dich jemals gefragt, wie wir aus Wasser Wasserstoff gewinnen können? Die Elektrolyse ist der Schlüssel zu dieser faszinierenden Technologie. Sie spielt eine entscheidende Rolle in der modernen Energieproduktion und bietet uns eine umweltfreundliche Möglichkeit, Wasserstoff zu erzeugen.
In diesem Artikel werden wir die Grundlagen der Elektrolyse erkunden, ihre Anwendungen in der Industrie und ihre Bedeutung für die nachhaltige Energiezukunft. Wir zeigen, wie dieser Prozess nicht nur die Energieerzeugung revolutioniert, sondern auch zur Reduzierung von Treibhausgasemissionen beiträgt.
Was Ist Elektrolyse?
Elektrolyse ist ein elektrochemischer Prozess, der die Zerlegung von Verbindungen durch elektrischen Strom ermöglicht. Diese Technik findet in verschiedenen Anwendungen Verwendung, besonders in der Gewinnung von Wasserstoff. Wir verstehen elektrolytische Prozesse als essentiell für nachhaltige Energielösungen.
Elektrolyse erfolgt in mehreren Schritten:
In der Industrie nutzen wir verschiedene Elektrolyseverfahren:
Elektrolyse spielt eine Schlüsselrolle in unserer zukünftigen Energiestrategie, indem sie hilft, die Treibhausgasemissionen zu reduzieren und eine saubere Wasserstofferzeugung zu fördern. Diese Technologie hat das Potenzial, die Art und Weise zu revolutionieren, wie wir Energie erzeugen und nutzen.
Anwendungsgebiete Der Elektrolyse
Die Elektrolyse findet breite Anwendung in verschiedenen industriellen Bereichen, die für die Energieerzeugung und die Materialverarbeitung entscheidend sind.
Wasserstoffproduktion
Die Elektrolyse spielt eine zentrale Rolle bei der Produktion von Wasserstoff. Durch diesen Prozess kann grüner Wasserstoff gewonnen werden, indem Wassermoleküle in Wasserstoff- und Sauerstoffgas zerlegt werden. Dieser Wasserstoff hat unterschiedliche Anwendungsbereiche. Beispiele für die Nutzung sind:
Metallverarbeitung
In der Metallverarbeitung nutzt die Elektrolyse verschiedene Anwendungen, die die Materialeigenschaften verbessern. Die Elektrolyse wird zum Beispiel eingesetzt zur:
Diese Anwendungen zeigen, wie die Elektrolyse sowohl bei der Energieerzeugung als auch bei der Materialbearbeitung von Bedeutung ist.
Die Chemischen Grundlagen Der Elektrolyse
Die Elektrolyse ist ein komplexer elektrochemischer Prozess. Er zerlegt chemische Verbindungen durch den Einfluss elektrischer Energie.
Elektrolysezelle
In der Elektrolysezelle erfolgen die chemischen Reaktionen an zwei Elektroden: der Anode und der Kathode. Hier ist eine Übersicht der Hauptkomponenten:
- Elektroden: Diese bestehen aus leitfähigem Material, oft Graphit oder Metall.
- Elektrolyt: Eine ionenleitende Flüssigkeit, die die Bewegung von Ionen ermöglicht.
- Stromquelle: Sie liefert die notwendige elektrische Energie, um die Reaktionen auszulösen.
- Separator: Er trennt die Elektroden und verhindert Kurzschlüsse.
In der Zelle finden an der Anode Oxidationsreaktionen und an der Kathode Reduktionsreaktionen statt. Wenn elektrischer Strom fließt, bewegen sich die Ionen im Elektrolyten zur jeweiligen Elektrode.
Elektrolytlösungen
Die Auswahl der Elektrolytlösungen spielt eine entscheidende Rolle für die Effizienz der Elektrolyse. Unterschiedliche Lösungen fördern spezifische Reaktionen. Die wichtigsten Arten sind:
- Alkalische Lösungen: Diese enthalten Kaliumhydroxid oder Natriumhydroxid und fördern die Wasserstoffproduktion.
- Säurelösungen: Hier eignen sich Schwefelsäure oder Salzsäure, um die Effektivität zu steigern.
- Salzlösungen: Sie bestehen aus Salzen wie Natriumchlorid und verbessern die Leitfähigkeit.
Die Wahl der Elektrolytlösung beeinflusst die Reaktionsgeschwindigkeit und die Reinheit der Produkte. Anhand dieser Faktoren optimieren wir die Produktionsbedingungen, um die gewünschten Ergebnisse zu erzielen.
Vor- Und Nachteile Der Elektrolyse
Die Elektrolyse bietet zahlreiche Vorteile, die sie zu einer attraktiven Technologie für verschiedene Anwendungen machen:
Allerdings gibt es auch Nachteile, die bei der Anwendung der Elektrolyse berücksichtigt werden sollten:
Die Abwägung zwischen diesen Vorteilen und Nachteilen ist entscheidend, um die geeigneten Anwendungen der Elektrolyse in der Zukunft zu bestimmen.
Fazit
Elektrolyse ist mehr als nur ein chemischer Prozess. Sie ist ein entscheidender Baustein für eine nachhaltige Energiezukunft. Durch die Produktion von grünem Wasserstoff eröffnet sie zahlreiche Möglichkeiten in verschiedenen Industrien und trägt zur Verringerung von Treibhausgasemissionen bei.
Die Flexibilität und Effizienz der Elektrolyse machen sie zu einer attraktiven Lösung für die Herausforderungen der Energieerzeugung. Trotz der bestehenden Herausforderungen wie hohe Investitionskosten und technologische Hürden bleibt ihr Potenzial unbestreitbar.
Wir sollten die Entwicklungen in der Elektrolyse aufmerksam verfolgen und innovative Ansätze unterstützen. Nur so können wir die Vorteile dieser Technologie optimal nutzen und eine saubere und nachhaltige Energiezukunft gestalten.