Ionensubstanzen spielen eine entscheidende Rolle in vielen Bereichen unseres Lebens. Diese chemischen Verbindungen sind nicht nur faszinierend sondern auch äußerst vielseitig. In unserem Artikel werden wir die Eigenschaften von Ionensubstanzen näher beleuchten und deren Anwendungen in der Industrie sowie im Alltag erkunden.
Wir erfahren, wie Ionensubstanzen in unterschiedlichen Prozessen eingesetzt werden und welche Beispiele es für ihre Nutzung gibt. Von der Wasseraufbereitung bis zur Elektrochemie zeigen sie sich als unverzichtbare Bestandteile moderner Technologien. Haben Sie sich schon einmal gefragt, wie diese Substanzen unsere Umwelt beeinflussen oder welche innovativen Lösungen sie bieten können? Lassen Sie uns gemeinsam eintauchen in die Welt der Ionensubstanzen und deren spannende Möglichkeiten entdecken!
Eigenschaften von Ionensubstanzen
Ionensubstanzen zeichnen sich durch eine Reihe von besonderen Eigenschaften aus, die sie von anderen chemischen Verbindungen unterscheiden. Diese Eigenschaften sind entscheidend für ihre Anwendung in verschiedenen Bereichen, einschließlich der Industrie und Forschung. Die elektrische Leitfähigkeit ist eine der herausragenden . In geschmolzenem Zustand oder in Lösung können sie elektrische Ströme leiten, da die Ionen mobil sind und sich frei bewegen können.
Zusätzlich besitzen Ionensubstanzen oft hohe Schmelz- und Siedepunkte, was auf die starke Anziehungskraft zwischen den positiv und negativ geladenen Ionen zurückzuführen ist. Diese ionischen Bindungen erfordern erhebliche Mengen an Energie, um gebrochen zu werden.
Löslichkeit
Ein weiterer wichtiger Aspekt ist die Löslichkeit von Ionensubstanzen in Wasser. Viele dieser Substanzen lösen sich gut in polaren Lösungsmitteln wie Wasser aufgrund der Wechselwirkungen zwischen den Wassermolekülen und den Ionen. Zu den geläufigsten Beispielen zählen:
- Natriumchlorid (NaCl)
- Kaliumbromid (KBr)
- Magnesiumsulfat (MgSO₄)
Diese Substanzen zeigen unterschiedliche Löslichkeiten, die durch Faktoren wie Temperatur und Druck beeinflusst werden.
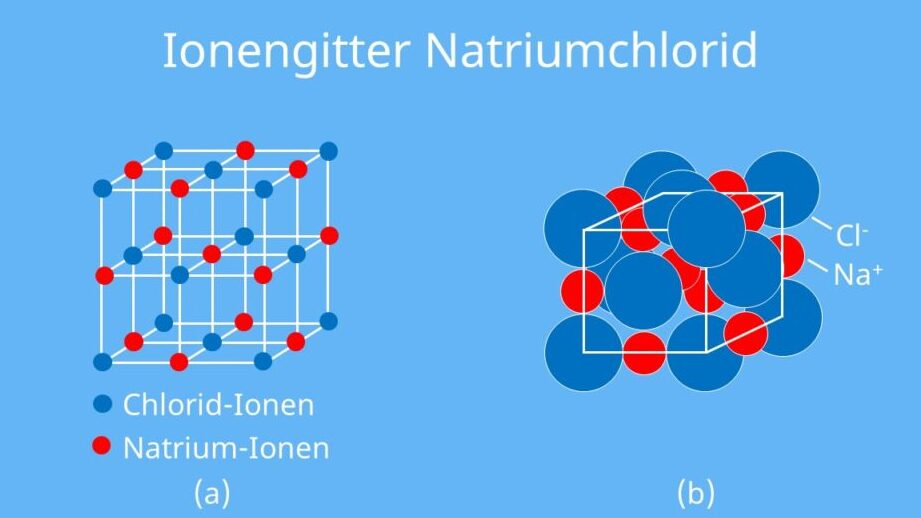
Kristallstruktur
Die Kristallstruktur von Ionensubstanzen spielt ebenfalls eine bedeutende Rolle bei ihren physikalischen Eigenschaften. Sie bilden typischerweise kristalline Gitterstrukturen, was zur Stabilität des Materials beiträgt. Die Anordnung der Ionen im Kristallgitter kann stark variieren, was zu unterschiedlichen physikalischen Eigenschaften führt:
| Ionensubstanz | Strukturtyp | Beispiel |
|---|---|---|
| Natriumchlorid | kubisch | NaCl |
| Calciumfluorid | kubisch | CaF₂ |
| Zinkblende | tetraedrisch | ZnS |
Die spezifische Struktur beeinflusst nicht nur das Aussehen einer Ionensubstanz, sondern auch deren Reaktivität und mechanische Festigkeit.
Insgesamt ergeben diese Eigenschaften ein umfassendes Bild davon, warum Ionensubstanzen so vielseitig eingesetzt werden können und welche Bedeutung sie in Wissenschaft und Technik haben.
Anwendungen in der Industrie und Forschung
Die Anwendungen von Ionensubstanzen in der Industrie und Forschung sind vielfältig und entscheidend für zahlreiche technologische Fortschritte. Aufgrund ihrer besonderen Eigenschaften, wie die hohe elektrische Leitfähigkeit, die Stabilität unter extremen Bedingungen sowie ihre Löslichkeit in Wasser, finden sie in verschiedenen Bereichen Anwendung. In der chemischen Industrie werden Ionensubstanzen häufig als Katalysatoren oder Reagenzien eingesetzt, um chemische Reaktionen zu beschleunigen oder bestimmte Produkte herzustellen.
Industrielle Anwendungen
In der industriellen Produktion spielen Ionensubstanzen eine zentrale Rolle. Sie werden beispielsweise in der Wasseraufbereitung verwendet, um unerwünschte Ionen aus dem Wasser zu entfernen und somit dessen Qualität zu verbessern. Außerdem kommen sie in der Batterietechnologie zum Einsatz; Lithium-Ionen-Batterien sind ein bekanntes Beispiel dafür. Diese Batterien nutzen ionische Verbindungen zur Speicherung und Freisetzung von Energie, was sie effizient und langlebig macht.
Ein weiterer bedeutender Bereich ist die Düngerherstellung, wo ionische Salze als Nährstoffquellen dienen. Zu den häufig verwendeten Substanzen gehören:
- Ammoniumchlorid (NH₄Cl)
- Kaliumsulfat (K₂SO₄)
- Calciumphosphat (Ca₃(PO₄)₂)
Diese Dünger fördern das Pflanzenwachstum durch Bereitstellung essentieller Nährstoffe.
Forschungseinsatz
In der Forschung sind Ionensubstanzen ebenfalls von großer Bedeutung. Sie werden genutzt, um neue Materialien mit spezifischen Eigenschaften zu entwickeln oder bestehende Materialien zu optimieren. Besonders erwähnenswert ist ihr Einsatz in der Materialwissenschaft, wo Forscher versuchen, ionische Verbindungen für die Entwicklung innovativer Elektronikkomponenten zu nutzen.
Darüber hinaus spielen Ionensubstanzen eine Schlüsselrolle in biochemischen Experimenten und Analysen. Ihre Fähigkeit, Ionenwechselwirkungen präzise zu steuern und nachzuweisen, ermöglicht es Wissenschaftlern, komplexe biologische Systeme besser zu verstehen.
| Anwendungsbereich | Ionensubstanz | Beispiel |
|---|---|---|
| Batterietechnologie | Lithiumionenverbindung | LiCoO₂ (Lithiumcobaltoxid) |
| Düngerherstellung | Kaliumnitrat | KNO₃ (Kaliumsalpeter) |
| Wasseraufbereitung | Natriumhydroxid | NaOH (Ätznatron) |
Zusammenfassend lässt sich sagen, dass die breite Palette an Anwendungen von Ionensubstanzen sowohl industrielle Prozesse als auch wissenschaftliche Forschungen maßgeblich beeinflusst und verbessert hat.
Beispiele für Ionensubstanzen in der Natur
In der Natur finden wir eine Vielzahl von Ionensubstanzen, die nicht nur für das ökologische Gleichgewicht wichtig sind, sondern auch für zahlreiche biologische Prozesse. Diese ionischen Verbindungen sind in verschiedenen Formen und Zusammensetzungen vorhanden und spielen eine entscheidende Rolle im Lebenszyklus vieler Organismen. Wir möchten einige herausragende Beispiele vorstellen, die verdeutlichen, wie weit verbreitet und bedeutend Ionensubstanzen in unserer Umwelt sind.
Mineralien
Ein bekanntes Beispiel für Ionensubstanzen in der Natur sind Mineralien, die aus ionischen Verbindungen bestehen. In Gesteinen finden sich häufig Salze wie Natriumchlorid (NaCl) oder Kalziumkarbonat (CaCO₃). Diese Mineralien haben nicht nur Einfluss auf geochemische Prozesse, sondern auch auf die Bildung von Böden und Ökosystemen.
Salzwasser
Ein weiteres eindrucksvolles Beispiel ist das Salzwasser der Ozeane. Es enthält hochkonzentrierte Lösungen von Ionen wie Natrium (Na⁺), Chlorid (Cl⁻) und Magnesium (Mg²⁺). Diese Ionen beeinflussen das marine Leben erheblich, da viele Organismen spezielle Anpassungen entwickelt haben, um mit den hohen Salzkonzentrationen zurechtzukommen.
Biochemische Prozesse
Ionensubstanzen spielen auch eine fundamentale Rolle in biochemischen Prozessen innerhalb lebender Zellen. Zum Beispiel werden Calciumionen (Ca²⁺) als Signalmoleküle verwendet, um verschiedene physiologische Reaktionen zu steuern. Auch Kalium- (K⁺) und Natriumionen sind entscheidend für die Aufrechterhaltung des Membranpotentials in Nervenzellen.
Die Vielfalt der Ionensubstanzen zeigt sich also nicht nur in ihrer chemischen Struktur, sondern auch in ihren zahlreichen Funktionen innerhalb natürlicher Systeme. Sie tragen zur Stabilität biologischer Prozesse bei und unterstützen das Gleichgewicht ökologischer Gemeinschaften weltweit.
Die Rolle von Ionenverbindungen in biochemischen Prozessen
Ionensubstanzen sind für eine Vielzahl biochemischer Prozesse in lebenden Organismen unverzichtbar. Sie tragen nicht nur zur Aufrechterhaltung der Zellstruktur bei, sondern sind auch entscheidend für die Signalübertragung und den Stoffwechsel. Ionen wie Natrium (Na⁺), Kalium (K⁺) und Calcium (Ca²⁺) spielen zentrale Rollen in physiologischen Reaktionen, die für das Funktionieren des Körpers unerlässlich sind.
Signalübertragung
Ein bemerkenswertes Beispiel ist die Rolle von Calciumionen in der Signalübertragung. Diese Ionen fungieren als sekundäre Botenstoffe, die verschiedene zelluläre Aktivitäten steuern, einschließlich Muskelkontraktion und Neurotransmitterfreisetzung. Der Anstieg von Ca²⁺-Ionen innerhalb der Zelle kann eine Kaskade von Reaktionen auslösen, die letztlich zu einer spezifischen zellulären Antwort führen.
Membranpotenzial
Darüber hinaus beeinflussen Ionenverbindungen das Membranpotenzial von Zellen erheblich. In Nervenzellen beispielsweise sorgt ein ausgewogenes Verhältnis zwischen Na⁺- und K⁺-Ionen für die Erzeugung elektrischer Impulse, die für die Kommunikation zwischen Neuronen notwendig sind. Dieses Gleichgewicht wird durch spezielle Transportproteine aufrechterhalten, welche aktiv Ionen über Zellmembranen pumpen.
| Ionentyp | Funktion |
|---|---|
| Na⁺ | Wichtig für Nervenimpulse |
| K⁺ | Regulierung des Ruhepotenzials |
| Ca²⁺ | Signalmolekül |
Enzymatische Aktivität
Zusätzlich spielen ionenspezifische Verbindungen eine Rolle als Cofaktoren in enzymatischen Reaktionen. Viele Enzyme benötigen Metallionen wie Magnesium (Mg²⁺) oder Zink (Zn²⁺), um ihre katalytische Aktivität zu entfalten. Diese Ionensubstanzen stabilisieren nicht nur die Struktur des Enzyms, sondern ermöglichen auch präzise chemische Reaktionen im Stoffwechsel.
Die vielfältigen Funktionen von Ionenverbindungen zeigen sich also eindrucksvoll in den komplexen biochemischen Prozessen unseres Körpers. Ihre essentielle Beteiligung an lebenswichtigen Vorgängen unterstreicht nicht nur ihre Bedeutung im biologischen Kontext, sondern macht sie auch zu einem zentralen Thema unserer Forschung über Ionensubstanzen und deren Anwendungen.
Unterschiede zwischen ionischen und kovalenten Verbindungen
Die sind fundamental für das Verständnis von Ionensubstanzen und deren Eigenschaften. Während ionische Verbindungen durch die elektrostatische Anziehung zwischen positiv und negativ geladenen Ionen entstehen, basieren kovalente Verbindungen auf der gemeinsamen Nutzung von Elektronenpaaren zwischen Atomen. Diese grundlegenden Unterschiede führen zu variierenden physikalischen und chemischen Eigenschaften.
Ein entscheidender Aspekt ist die Bindungsstärke. In ionischen Verbindungen sind die Bindungen in der Regel stark, was zu hohen Schmelz- und Siedepunkten führt. Im Gegensatz dazu können kovalente Bindungen schwächer sein, was sich in niedrigeren Schmelz- und Siedepunkten äußern kann.
Zusätzlich unterscheiden sich beide Verbindungstypen hinsichtlich ihrer Löslichkeit in Wasser. Ionische Verbindungen neigen dazu, gut in polarer Lösung wie Wasser löslich zu sein, während viele kovalente Substanzen schlecht wasserlöslich sind oder nur unter bestimmten Bedingungen lösen.
| Eigenschaft | Ionische Verbindungen | Kovalente Verbindungen |
|---|---|---|
| Bindungsart | Elektrostatische Anziehung | Gemeinsame Elektronennutzung |
| Schmelzpunkt | Hoch | Variabel |
| Löslichkeit in Wasser | Hoch | Niedrig bis variabel |
| elektrische Leitfähigkeit | Gut (in geschmolzenem Zustand) | Gering bis nicht leitend |
Ein weiterer wichtiger Unterschied ist die elektrische Leitfähigkeit: Ionische Verbindungen leiten elektrischen Strom im geschmolzenen Zustand oder wenn sie gelöst sind, da die Ionen mobil werden. Kovalente Verbindungen hingegen zeigen normalerweise eine schlechte elektrische Leitfähigkeit, da sie keine freien Ladungsträger besitzen.
Diese Differenzierungen helfen uns nicht nur beim Verständnis der Struktur und Funktion von Materialien, sondern auch bei der Anwendung von Ionensubstanzen in verschiedenen Bereichen wie Chemie, Biologie und Materialwissenschaften.