Isotope sind faszinierende Elemente, die in der Natur überall um uns herum vorkommen. Aber was genau sind Isotope und warum sind sie so wichtig? In diesem Artikel werden wir verschiedene Isotope Beispiele erkunden, die uns helfen, die Bedeutung dieser chemischen Varianten besser zu verstehen.
Was Sind Isotope?
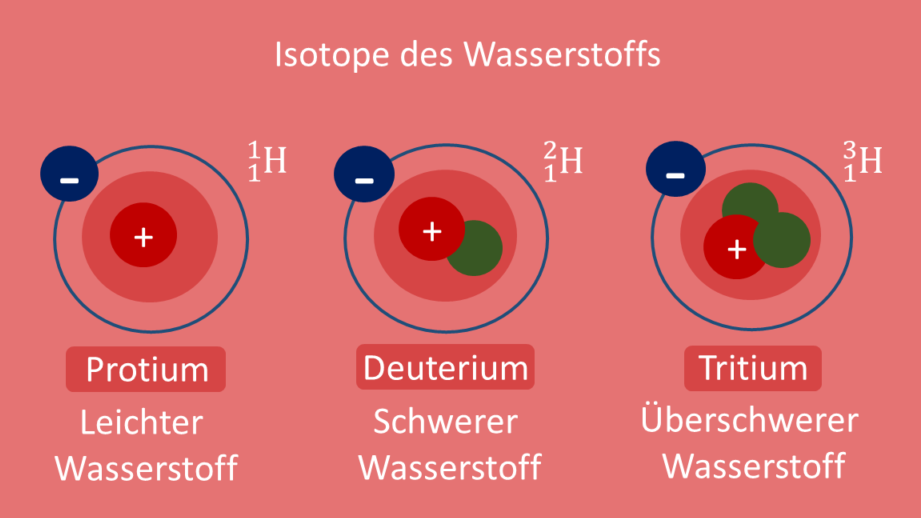
Isotope sind Varianten eines chemischen Elements, die die gleiche Anzahl an Protonen, jedoch unterschiedliche Neutronenzahlen besitzen. Diese Unterschiede beeinflussen die Masse des Elements, nicht aber seine chemischen Eigenschaften. Isotope spielen eine wichtige Rolle in vielen Bereichen, wie der Medizin, der Archäologie und der Energieerzeugung.
Wir erkennen verschiedene Arten von Isotopen, einschließlich:
Die Nutzung von Isotopen in der Medizin revolutionierte die diagnostischen Verfahren und Behandlungen. Beispielsweise ermöglichen radioaktive Isotope wie Iod-131 ((^{131}text{I})) die gezielte Behandlung von Schilddrüsenerkrankungen.
In der Archäologie verwenden Forscher stabile Isotope, um das Alter von organischen Materialien zu bestimmen. Die Bestimmung des Alters von Funden mit Kohlenstoff-14 bietet wertvolle Einblicke in vergangene Kulturen.
Die Energieerzeugung nutzt Uran-Isotope, um Kernreaktoren zu betreiben. Diese Technologien bieten eine alternative Energiequelle und reduzieren die Abhängigkeit von fossilen Brennstoffen.
Beispiele Für Isotope
Wir betrachten verschiedene Beispiele für Isotope, die in der Wissenschaft und Industrie von Bedeutung sind. Diese konkreten Fälle zeigen, wie vielseitig Isotope eingesetzt werden.
Stabile Isotope
Stabile Isotope sind solche, die nicht radioaktiv sind und deshalb keine Strahlung abgeben. Sie bleiben über lange Zeit unverändert. Einige Beispiele sind:
Diese stabilen Isotope finden Anwendung in der Altersbestimmung von organischen Materialien oder in der Biochemie.
Instabile Isotope
Instabile Isotope hingegen sind radioaktiv und zerfallen über Zeit in andere Elemente. Beispiele für instabile Isotope sind:
Diese instabilen Isotope sind entscheidend für medizinische Anwendungen, Energietechnologien und Forschung.
Anwendungen Von Isotopen
Isotope haben vielfältige Anwendungen in verschiedenen Bereichen. Besonders hervorzuheben sind die medizinischen und industriellen Anwendungen, die uns eindrucksvoll zeigen, wie wichtig Isotope in unserem Alltag sind.
Medizinische Anwendungen
In der Medizin spielen Isotope eine entscheidende Rolle. Hier sind einige Hauptanwendungen:
- Diagnostik: Radioaktive Isotope wie ^99mTc werden in der Bildgebung eingesetzt, um Organe und Gewebe darzustellen.
- Therapie: Isotope wie ^131I behandeln Schilddrüsenerkrankungen durch gezielte Strahlentherapie.
- Radiokohlenstoffdatierung: ^14C hilft, das Alter von biologischem Material zu bestimmen, was für archäologische Studien wichtig ist.
- Tracers: Isotope verfolgen Stoffwechselprozesse im Körper, was für die Forschung von Bedeutung ist.
Industrielle Anwendungen
Auch in der Industrie finden Isotope breite Anwendung. Hier einige wichtige Bereiche:
- Strahlenmessung: Isotope wie ^137Cs werden in Strahlungsdetektoren eingesetzt, um Sicherheitsstandards zu gewährleisten.
- Materialprüfung: Isotope helfen bei der Analyse von Werkstoffen durch zerstörungsfreie Prüfmethoden.
- Alterungsstudien: Stabilen Isotopen wie ^18O verwenden wir zur Untersuchung von Wasserquellen und Klimaveränderungen.
- Energieerzeugung: Uran-Isotope ^235U und ^238U dienen in Kernkraftwerken zur Energieproduktion.
Die vielseitige Nutzung von Isotopen in der Medizin und Industrie verdeutlicht deren immense Bedeutung für Fortschritt und Innovation.
Bedeutung Von Isotopen In Der Forschung
Isotope spielen in der Forschung eine entscheidende Rolle, da ihre einzigartige Eigenschaften vielfältige Anwendungsmöglichkeiten bieten. Sie sind nicht nur in den Naturwissenschaften wichtig, sondern auch in der Medizin, Archäologie und Umweltwissenschaft. Hier sind einige Schlüsselpunkte zur Bedeutung von Isotopen in der Forschung:
Durch die Anwendung von Isotopen erlangen wir neue Erkenntnisse und entwickeln innovative Techniken. Diese Vielfalt zeigt, wie wichtig das Verständnis von Isotopen für Fortschritte in verschiedenen Wissenschaftsbereichen ist.
Fazit
Isotope sind nicht nur faszinierende chemische Varianten sondern auch unverzichtbare Werkzeuge in vielen Bereichen. Ihre Anwendungen in der Medizin und Industrie zeigen eindrucksvoll, wie sie unser Verständnis von Wissenschaft und Technologie erweitern.
Durch die Erforschung stabiler und radioaktiver Isotope können wir bedeutende Fortschritte in der Diagnostik und Therapie erzielen. Zudem tragen sie zur Lösung drängender Fragen in der Umweltforschung und Archäologie bei.
Das Wissen über Isotope eröffnet uns neue Perspektiven und Möglichkeiten in der Forschung. Wir sollten die Vielseitigkeit und Bedeutung von Isotopen weiterhin erkunden und ihre Potenziale nutzen.