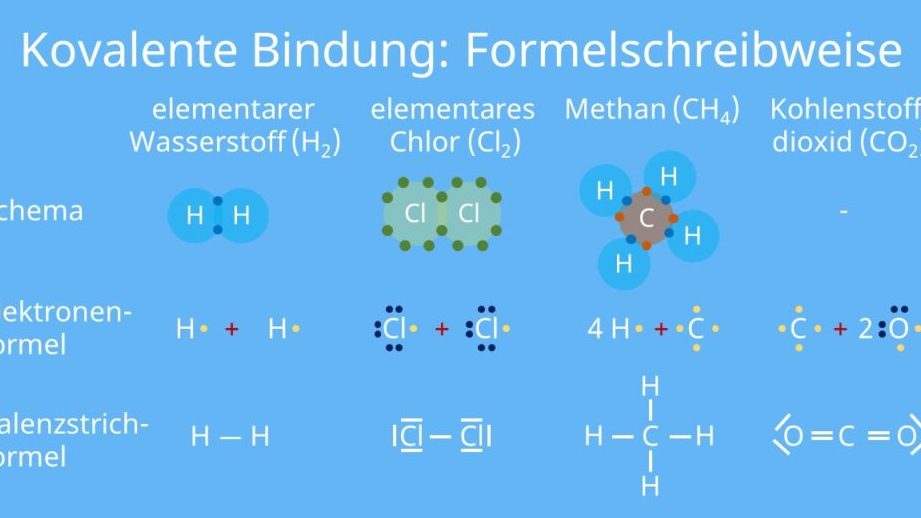
Kovalente Bindungen sind das Herzstück der Chemie und spielen eine entscheidende Rolle in der Struktur und Funktion von Molekülen. Wie entstehen diese Bindungen und warum sind sie so wichtig für das Leben, wie wir es kennen? In diesem Artikel tauchen wir tief in die faszinierende Welt der kovalenten Bindung ein und erkunden, wie Atome durch das Teilen von Elektronen stabile Verbindungen eingehen.
Was Ist Eine Kovalente Bindung?
Eine kovalente Bindung entsteht, wenn zwei Atome Elektronen teilen. Diese Art der Bindung führt häufig zu stabilen Molekülen, die für die chemischen Strukturen von Stoffen entscheidend sind. Unsere Umgebung besteht aus zahlreichen Molekülen, die durch kovalente Bindungen zusammengehalten werden.
Die wesentlichen Merkmale der kovalenten Bindung sind:
Kovalente Bindungen spielen eine zentrale Rolle in biologischen Molekülen, wie Proteinen und Nukleinsäuren. Zudem beeinflussen sie die physikalischen Eigenschaften von Stoffen, wie Schmelz- oder Siedepunkte. Wir sehen also, dass kovalente Bindungen essenziell für das Verständnis der Chemie und das Leben im Allgemeinen sind.
Eigenschaften Kovalenter Bindungen
Kovalente Bindungen zeigen spezifische Eigenschaften, die für das Verständnis ihrer Rolle in der Chemie wichtig sind. Dazu zählen Aspekte wie die Bindungsstärke und die Polarität von Molekülen.
Elektronegativität und Bindungsstärke
Die Elektronegativität von Atomen beeinflusst die Stärke kovalenter Bindungen. Höhere Elektronegativität führt oft zu stärkeren Bindungen. Bei der Betrachtung von Bindungsstärken identifizieren wir verschiedene Faktoren:
Starke Bindungen stabilisieren Moleküle, während schwächere Bindungen in verschiedenen chemischen Reaktionen leichter aufgebrochen werden können.
Polarität von Molekülen
Die Polarität von Molekülen resultiert aus der ungleichen Verteilung von Elektronen. Moleküle können polar oder unpolar sein, was ihre Eigenschaften und ihr Verhalten in chemischen Reaktionen beeinflusst.
Diese Eigenschaften sind entscheidend für das Verhalten von Molekülen in Lösung, ihre Interaktionen und die Bildung von Wasserstoffbrücken.
Beispiele Für Kovalente Bindungen
Kovalente Bindungen sind in vielen Molekülen zu finden, und sie sind entscheidend für deren Struktur und Eigenschaften. Wir betrachten hier einige spezifische Arten von kovalenten Bindungen.
Einfach- und Doppelbindungen
Einfach- und Doppelbindungen bilden die Grundlage vieler chemischer Verbindungen.
Wir sehen, dass die Art der Bindung die Eigenschaften und die Reaktivität der Moleküle beeinflusst.
Trippelbindungen und Ihre Bedeutung
Trippelbindungen sind besonders stark und führen zu stabilen Molekülen.
Trippelbindungen tragen somit nicht nur zur Stabilität bei, sondern auch zur Vielfalt von chemischen Reaktionen, die wir in der Chemie beobachten.
Kovalente Bindungen In Der Chemischen Industrie
Kovalente Bindungen spielen eine entscheidende Rolle in der chemischen Industrie. Sie beeinflussen wesentlich die Eigenschaften von Materialien und deren Anwendungen. Hier sind einige Bereiche, in denen kovalente Bindungen besonders wichtig sind:
Kovalente Bindungen bestimmen auch die physikalischen Eigenschaften von Materialien. Hierzu zählen:
Die Flexibilität und Stabilität kovalenter Bindungen macht sie unverzichtbar in der Entwicklung neuer Produkte und Technologien. In der chemischen Industrie ist das Verständnis dieser Bindungen der Schlüssel zu Innovation und Fortschritt.
Fazit
Kovalente Bindungen sind das Herzstück der chemischen Interaktionen und prägen die Welt um uns herum. Sie ermöglichen die Bildung stabiler Moleküle und beeinflussen entscheidend die Eigenschaften von Materialien. Durch das Verständnis dieser Bindungen können wir die Komplexität biologischer Systeme und die Vielfalt chemischer Reaktionen besser nachvollziehen.
Die Bedeutung kovalenter Bindungen erstreckt sich über die Grundlagen der Chemie hinaus und spielt eine zentrale Rolle in der Industrie und Technologie. Indem wir die Mechanismen hinter diesen Bindungen erforschen, eröffnen sich neue Möglichkeiten für Innovation und Fortschritt. Lassen wir uns von der faszinierenden Welt der kovalenten Bindungen inspirieren und ihre Anwendungen weiter entdecken.