Die Mesomerie ist ein faszinierendes Konzept in der Chemie, das uns hilft, die Stabilität und Struktur von Molekülen besser zu verstehen. In diesem Artikel werden wir verschiedene Mesomerie Beispiele untersuchen und ihre Anwendungen im Detail erläutern. Durch die Analyse realer Verbindungen zeigen wir, wie Mesomerie zur Erklärung chemischer Eigenschaften beiträgt.
Wir möchten herausfinden, wie unterschiedliche Resonanzstrukturen entstehen und welche Bedeutung sie für die chemische Stabilität haben. Wussten Sie, dass viele organische Verbindungen durch Mesomerie stabilisiert werden? Diese Erkenntnisse sind nicht nur theoretisch relevant sondern auch praktisch wichtig für die Entwicklung neuer Materialien und Medikamente. Lassen Sie uns gemeinsam in die Welt der Mesomerie eintauchen und entdecken, warum diese Konzepte so entscheidend für unser Verständnis der Chemie sind. Was erwarten Sie von den folgenden Beispielen?
Mesomerie Beispiele in der Chemie
Die Mesomerie spielt eine entscheidende Rolle in der Chemie, insbesondere bei der Stabilität und Reaktivität von Molekülen. In diesem Abschnitt werden wir einige Mesomerie Beispiele aus verschiedenen chemischen Substanzen betrachten und deren Bedeutung für die strukturelle Integrität und Eigenschaften untersuchen. Diese Beispiele verdeutlichen nicht nur die Theorie der Mesomerie, sondern auch ihre praktische Anwendbarkeit in der organischen Chemie.
Aromatische Verbindungen
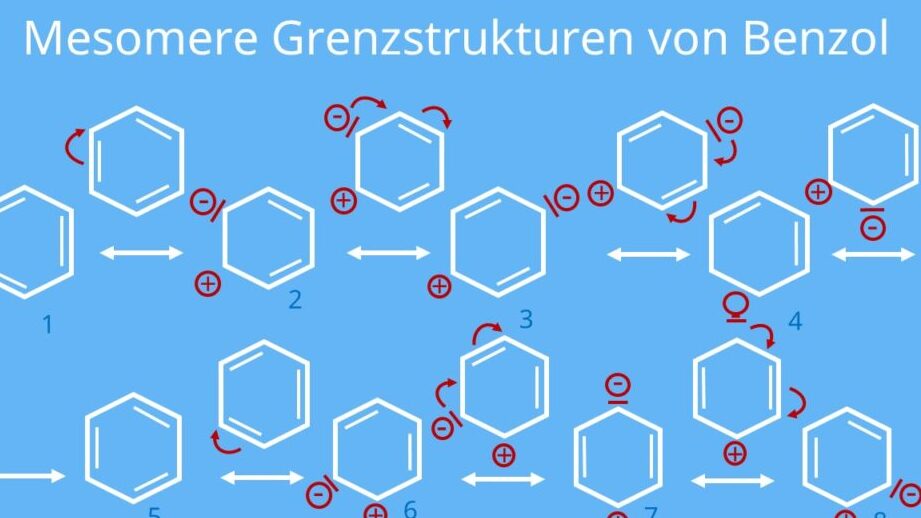
Aromatische Verbindungen sind klassische Beispiele für Mesomerie. Nehmen wir Benzol als Beispiel:
- Benzol (C6H6):
- Es hat eine ringförmige Struktur mit sechs Kohlenstoffatomen.
- Die Elektronen in den Doppelbindungen sind delokalisiert, was zu einer erhöhten Stabilität führt.
| Strukturformel | Beschreibung |
|---|---|
| !Benzol-Struktur | Benzol zeigt Mesomerie durch die delokalisierten π-Elektronen. |
Diese Delokalisierung ist entscheidend für die besondere Stabilität des Benzols im Vergleich zu anderen ungesättigten Verbindungen.
Carbonsäuren
Ein weiteres Beispiel finden wir in den Carbonsäuren, wie der Essigsäure:
- Essigsäure (CH3COOH):
- Sie zeigt zwei Resonanzstrukturen, wobei das Proton zwischen dem Hydroxyl- und dem Carbonylkohlenstoff delokalisiert wird.
| Strukturformel | Beschreibung |
|---|---|
| !Essigsäure-Struktur | Essigsäure hat zwei Resonanzformen, die zur Stabilisierung beitragen. |
Diese Resonanz erklärt die chemischen Eigenschaften von Carbonsäuren sowie deren Verhalten in Reaktionen.
Ionenverbindungen
Schließlich können auch Ionenverbindungen mesomere Charakteristika aufweisen:
- Nitrat-Ion (NO3-):
- Das Nitrat-Ion hat mehrere Resonanzstrukturen, was seine hohe Stabilität erklärt.
| Strukturformel | Beschreibung |
|---|---|
| !Nitrat-Ion-Struktur | Nitrat-Ion zeigt Mesomerie durch drei gleichwertige Resonanzstrukturen. |
Jede dieser Strukturen trägt zur Gesamtstabilität des Ions bei und beeinflusst dessen chemisches Verhalten.
In all diesen Beispielen sehen wir deutlich, dass die Mesomerie nicht nur ein theoretisches Konzept ist, sondern einen wesentlichen Einfluss auf die Eigenschaften und Reaktivitäten von Molekülen hat.
Anwendung von Mesomerie in organischen Verbindungen
Die ist ein zentrales Konzept, das unser Verständnis der chemischen Stabilität und Reaktivität vertieft. In dieser Sektion werden wir untersuchen, wie die Mesomerie in verschiedenen organischen Molekülen zum Tragen kommt und welche Auswirkungen dies auf ihre Eigenschaften hat. Durch diese Analyse wird deutlich, dass die Mesomerie Beispiele nicht nur theoretisch sind, sondern auch praktische Relevanz besitzen.
Alkohole
Alkohole zeigen ebenfalls mesomere Eigenschaften, die sich auf ihre chemische Aktivität auswirken können. Ein gutes Beispiel hierfür ist:
- Ethanol (C2H5OH):
- Es kann zwei Resonanzstrukturen bilden, in denen das Hydroxyl-Oxygen delokalisiert ist.
| Strukturformel | Beschreibung |
|---|---|
| !Ethanol-Struktur | Ethanol zeigt Mesomerie durch delokalisierte Elektronen im Hydroxylbereich. |
Diese Delokalisierung trägt zur Stabilisierung des Moleküls bei und beeinflusst seine Wechselwirkungen mit anderen chemischen Substanzen.
Ketone
Ketone sind eine weitere Klasse von Verbindungen, bei denen die Mesomerie eine wichtige Rolle spielt. Ein Beispiel dafür ist:
- Aceton (C3H6O):
- Aceton hat zwei Hauptresonanzstrukturen, was zu seiner Stabilität beiträgt.
| Strukturformel | Beschreibung |
|---|---|
| !Aceton-Struktur | Aceton zeigt Mesomerie durch delokalisierte π-Elektronen am Carbonyl-C. |
Die Fähigkeit des Acetons zur Bildung mehrerer Resonanzformen erklärt seine vielseitige Verwendung als Lösungsmittel in der Industrie.
Amine
Schließlich haben auch Amine mesomere Charakteristiken. Betrachten wir folgendes Beispiel:
- Anilin (C6H5NH2):
- Anilin zeigt mehrere Resonanzstrukturen aufgrund der Delokalisation der Elektronen zwischen dem Stickstoffatom und dem aromatischen Ring.
| Strukturformel | Beschreibung |
|---|---|
| !Anilin-Struktur | Anilin demonstriert Mesomerie durch die Interaktion zwischen den Elektronen des Aromaten und des Amino-Gruppen. |
Diese mesomeren Eigenschaften machen Anilin zu einem wichtigen Baustein in der organischen Synthese sowie in Farbstoffen.
In all diesen Beispielen erkennen wir klar, dass die Anwendung von Mesomerie nicht nur theoretischer Natur ist; sie spielt eine entscheidende Rolle für das Verständnis organischer Chemiekonzeptionen und deren praktischer Umsetzung.
Erklärungen zu Resonanzstrukturen und Stabilität
Die Resonanzstrukturen sind ein fundamentales Konzept im Bereich der Mesomerie, das uns hilft, die Stabilität verschiedener chemischer Verbindungen besser zu verstehen. Sie zeigen auf, wie Elektronen in Molekülen delokalisiert sind und somit zur Stabilität beitragen können. In dieser Sektion werden wir genauer untersuchen, wie Resonanzstrukturen gebildet werden und welchen Einfluss sie auf die Stabilität von Molekülen haben.
Ein wichtiges Beispiel für Resonanzstrukturen findet sich bei Benzol (C6H6). Benzol hat eine ringförmige Struktur mit einer speziellen Delokalisation der π-Elektronen:
- Benzol kann zwei Hauptresonanzformen darstellen.
- Diese Formen tragen zur besonderen Stabilität des Benzolmoleküls bei.
| Strukturformel | Beschreibung |
|---|---|
| !Benzol-Struktur | Benzol zeigt Mesomerie durch delokalisierte Elektronen im Ring, was seine besondere Stabilität erklärt. |
Zusätzlich ist es bemerkenswert, dass die Mesomerie Beispiele nicht nur theoretische Natur sind; sie spielen auch eine entscheidende Rolle in der Reaktivität von verschiedenen organischen Verbindungen. Zum Beispiel bei Ionen wie dem Nitrat-Ion (NO3⁻), wo drei verschiedene Resonanzstrukturen existieren:
- Jede Struktur trägt zur Gesamtstabilisierung des Ions bei.
- Die Delokalisation der Elektronen über mehrere Atome führt zu einer gleichmäßigen Verteilung der negativen Ladung.
| Strukturformel | Beschreibung |
|---|---|
| !Nitrat-Struktur | Nitrat-Ion zeigt mehrere Resonanzformen mit delokalisierten Elektronen zwischen den Sauerstoffatomen. |
Durch diese Betrachtungen wird deutlich, dass die Analyse von Resonanzstrukturen nicht nur theoretisch ist; sie bietet wertvolle Einblicke in die chemischen Eigenschaften und Reaktionen der Substanzen. Die mesomeren Eigenschaften ermöglichen es uns außerdem, Vorhersagen über das Verhalten von Molekülen unter bestimmten Bedingungen zu treffen und deren Reaktivität besser zu verstehen.
Bedeutung der Mesomerie für die Molekülgeometrie
Die Mesomerie hat einen erheblichen Einfluss auf die Molekülgeometrie, da sie die Verteilung der Elektronen innerhalb eines Moleküls beschreibt und somit dessen Struktur beeinflusst. Wenn wir über mesomere Effekte sprechen, ist es wichtig zu verstehen, dass diese Delokalisierung von Elektronen nicht nur die Stabilität erhöht, sondern auch die geometrische Anordnung der Atome in einem Molekül beeinflussen kann.
Ein gutes Beispiel dafür ist das Nitrat-Ion (NO3⁻), das wir bereits erwähnt haben. Die verschiedenen Resonanzstrukturen führen zu einer gleichmäßigen Verteilung der elektronischen Ladung und beeinflussen dadurch den Bindungswinkel zwischen den Sauerstoffatomen:
- Bindungswinkel: Im Nitrat-Ion beträgt der Bindungswinkel etwa 120 Grad, was auf eine trigonal-planare Geometrie hinweist.
- Delokalisierung: Diese Geometrie resultiert aus der delokalisierten Natur der π-Elektronen.
| Resonanzstruktur | Bindungswinkel |
|---|---|
| !Nitrat-Struktur | 120 Grad |
Zusätzlich zeigt uns die Betrachtung von Benzol erneut, wie Mesomerie die Molekülgeometrie prägt. Die delokalisierten π-Elektronen im Benzolring führen zur Ausbildung eines perfekten Sechsecks mit gleichen C-C-Bindungen:
- Gleichwertige Bindungen: Alle sechs C-C-Bindungen im Benzol sind gleich lang und stark.
- Planare Struktur: Dies führt zu einer planaren Geometrie des Moleküls.
Diese Beispiele verdeutlichen, dass mesomere Eigenschaften weitreichende Auswirkungen auf die physikalischen und chemischen Eigenschaften von Verbindungen haben können. Indem wir verstehen, wie Mesomerie unsere Modelle für Molekülgeometrien formt, können wir besser vorhersagen, wie diese Substanzen in unterschiedlichen Reaktionen agieren werden und welche stabilisierenden Effekte auftreten könnten.
Praktische Beispiele für Mesomerie in Alltagsstoffen
In unserem Alltag begegnen wir zahlreichen Stoffen, bei denen Mesomerie eine entscheidende Rolle spielt. Diese mesomeren Eigenschaften beeinflussen nicht nur die Stabilität der Moleküle, sondern auch deren physikalische und chemische Eigenschaften. Im Folgenden betrachten wir einige , um zu verdeutlichen, wie weitreichend diese Effekte sind.
1. Benzoesäure
Ein klassisches Beispiel ist die Benzoesäure, ein häufig verwendeter organischer Stoff in Lebensmitteln und der chemischen Industrie. Die benzoesäurehaltigen Moleküle zeigen mehrere Resonanzstrukturen:
- Resonanzstrukturen: Es existieren verschiedene Formen, die die delokalisierte Elektronenverteilung illustrieren.
- Stabilität: Diese Delokalisation führt zu einer erhöhten Stabilität des Moleküls im Vergleich zu einem isolierten strukturierten Ansatz.
| Resonanzstruktur | Stabilitätsbeitrag |
|---|---|
| !Benzoesäure-Struktur | Erhöhte Stabilität durch Delokalisierung |
2. Aspirin
Ein weiteres Beispiel finden wir im Schmerzmittel Aspirin (Acetylsalicylsäure), das als Antiinflammatorikum weit verbreitet ist. Hier zeigt sich ebenfalls eine bemerkenswerte Mesomerie:
- Delokalisierung: In der Struktur von Aspirin sind π-Elektronen zwischen den Aromaten und Carboxygruppen delokalisiert.
- Chemische Reaktivität: Diese Eigenschaft beeinflusst sowohl seine Reaktionsfähigkeit als auch seine Wechselwirkungen mit biologischen Zielstrukturen.
Die Resonanzstrukturen von Aspirin tragen zur Erklärung seiner Wirksamkeit und Nebenwirkungen bei.
3. Ethanol
Selbst in alltäglichen Substanzen wie Ethanol, dem Hauptbestandteil alkoholischer Getränke, zeigt sich ein mesomeres Verhalten:
- Hydroxylgruppe: Die Hydroxylgruppe (-OH) kann an verschiedenen Stellen innerhalb des Ethanolmoleküls agieren.
- Interaktionen: Diese mesomeren Eigenschaften ermöglichen Wechselwirkungen mit anderen Molekülen und beeinflussen so den Siedepunkt sowie die Löslichkeit.
Durch das Verständnis dieser praktischen Beispiele können wir erkennen, dass Mesomerie nicht nur theoretisch relevant ist, sondern auch erhebliche Auswirkungen auf unsere täglichen Erfahrungen mit chemischen Verbindungen hat.