Die Welt der Chemie ist faszinierend und voller Überraschungen. Ein zentrales Konzept, das wir oft in unseren Experimenten und Analysen begegnen, sind die Oxidationszahlen. Diese Zahlen spielen eine entscheidende Rolle bei der Bestimmung von Redoxreaktionen und helfen uns zu verstehen, wie Elektronen zwischen Atomen transportiert werden. In diesem Artikel werden wir die Definition, die Berechnung und die vielfältigen Anwendungen von Oxidationszahlen näher beleuchten.
Wir werden gemeinsam erkunden, wie man Oxidationszahlen ermittelt und welche Bedeutung sie in verschiedenen chemischen Prozessen haben. Warum sind diese Werte für Chemiker so wichtig? Wie beeinflussen sie unsere alltäglichen Anwendungen von Chemie? Wir laden Sie ein auf eine spannende Reise durch die Welt der Oxidationszahlen und hoffen Ihr Interesse für dieses wichtige Thema zu wecken!
Definition der Oxidationszahlen und ihre Bedeutung
Die Oxidationszahlen sind fundamentale Konzepte in der Chemie, die den Elektronenstatus von Atomen innerhalb einer chemischen Verbindung darstellen. Sie geben an, wie viele Elektronen ein Atom bei der Bildung von Bindungen gewinnt oder verliert. Diese Zahlen sind nicht nur nützlich für das Verständnis der chemischen Reaktionen, sondern auch entscheidend für die Klassifizierung und Analyse von Verbindungen. Durch die Bestimmung der Oxidationszahlen können wir die Art der Bindungen und den Transfer von Elektronen in Redoxreaktionen nachvollziehen.
Bedeutung der Oxidationszahlen
Die Bedeutung der Oxidationszahlen erstreckt sich über mehrere Bereiche:
- Identifikation von Redoxreaktionen: Die Kenntnis dieser Zahlen hilft uns zu erkennen, welche Atome oxidiert oder reduziert werden.
- Bestimmung des Molekülverhaltens: Bei komplexen Molekülen ermöglichen sie Vorhersagen über Stabilität und Reaktivität.
- Klassifizierung von Verbindungen: Sie unterstützen bei der Einordnung chemischer Verbindungen in Kategorien wie Salze, Säuren oder Basen.
Beispiele zur Verdeutlichung
Um die Anwendung der Oxidationszahlen besser zu verstehen, betrachten wir einige gängige Beispiele:
- In Wasser (H₂O) hat Wasserstoff eine Oxidationszahl von +1 und Sauerstoff -2.
- In Natriumchlorid (NaCl) trägt Natrium eine Oxidationszahl von +1 und Chlor -1.
Diese einfachen Beispiele zeigen deutlich, wie wichtig es ist, die richtigen Oxidationszahlen zu kennen, um das Verhalten einer Substanz vorherzusagen.
Zusammenfassung
Zusammenfassend lässt sich sagen, dass die Definition und Bedeutung der Oxidationszahlen in vielen Aspekten unseres Verständnisses chemischer Prozesse unverzichtbar sind. Sie bieten uns wertvolle Informationen über die elektronischen Eigenschaften von Atomen und deren Rolle in verschiedenen Reaktionen.
Berechnung von Oxidationszahlen in chemischen Verbindungen
Um die Oxidationszahlen in chemischen Verbindungen präzise zu berechnen, folgen wir einer Reihe von Regeln und Prinzipien. Diese Methoden erschließen uns den Elektronentransfer und die Bindungen zwischen Atomen. Der Prozess der Berechnung kann variieren, je nach Art der Verbindung und den beteiligten Elementen. Wir werden hier einige grundlegende Schritte erläutern, die uns dabei helfen.
Grundregeln zur Berechnung
- Reine Elemente: In ihrer elementaren Form haben alle Atome eine Oxidationszahl von 0.
- Einatomige Ionen: Die Oxidationszahl entspricht der Ladung des Ions (z.B. Na⁺ hat +1; Cl⁻ hat -1).
- Wasserstoff: In den meisten Verbindungen hat Wasserstoff eine Oxidationszahl von +1, außer in Metallhydriden, wo sie -1 beträgt.
- Sauerstoff: Sauerstoff hat normalerweise eine Oxidationszahl von -2, mit Ausnahmen wie in Peroxiden (-1) oder bei Fluorverbindungen (+2).
- Summe der Oxidationszahlen: Bei neutralen Molekülen ist die Summe aller Oxidationszahlen gleich 0; in polyatomaren Ionen entspricht sie der Ladung des Ions.
Diese Regeln bieten einen klaren Rahmen für unsere Berechnungen und ermöglichen es uns, systematisch an das Thema heranzugehen.
Beispielberechnung
Nehmen wir als Beispiel Sulfat (( text{SO}_4^{2-} )). Hier können wir die folgenden Schritte befolgen:
- Wir setzen die unbekannte Oxidationszahl von Schwefel als ( x ) fest.
- Da jeder Sauerstoff -2 trägt und es vier Sauerstoffe gibt, ergibt sich:
( x + 4(-2) = -2 )
- Das vereinfacht sich zu:
( x – 8 = -2 )
- Durch Umstellen erhalten wir:
( x = +6 )
Somit beträgt die Oxidationszahl des Schwefels im Sulfat +6.
Anwendung auf komplexe Moleküle
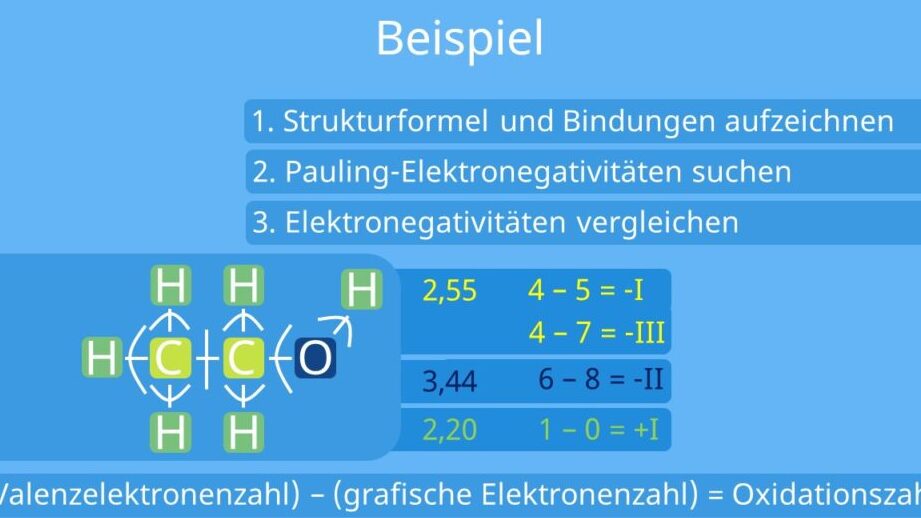
Bei komplexeren Molekülen ist es oft notwendig, eine strukturierte Analyse durchzuführen. Für organische Verbindungen beispielsweise können wir auch berücksichtigen:
- Die Elektronegativität der Atome
- Die Strukturformel zur Identifizierung funktioneller Gruppen
Diese Herangehensweise ermöglicht ein umfassenderes Verständnis dafür, wie sich Oxidationszahlen innerhalb einer Verbindung verhalten und welche Rolle sie bei chemischen Reaktionen spielen.
Durch diese methodische Herangehensweise an die Berechnung können wir sicherstellen, dass unsere Bestimmungen korrekt sind und somit unser Wissen über chemische Reaktionen erweitern.
Anwendungen von Oxidationszahlen in der Chemie
Die Oxidationszahlen spielen eine entscheidende Rolle in der Chemie, insbesondere bei der Analyse chemischer Reaktionen und der Bestimmung von Verbindungen. Sie helfen uns, die Elektronentransfers während dieser Reaktionen zu verstehen und bieten Einblicke in die Stabilität und Reaktivität verschiedener Moleküle. In diesem Abschnitt werden wir einige spezifische Anwendungen der Oxidationszahlen untersuchen.
Identifizierung von Redoxreaktionen
Ein wichtiger Anwendungsbereich ist die Identifizierung von Redoxreaktionen, bei denen es zu einer Übertragung von Elektronen zwischen Atomen kommt. Die Veränderung der Oxidationszahlen ermöglicht es uns, den Oxidationszustand eines Elements vor und nach einer Reaktion zu vergleichen:
- Oxidation
- Reduktion: Dies geschieht, wenn sich die Oxidationszahl verringert.
- Aktivitätsreihe: Wir können mit Hilfe von Oxidationszahlen vorhersagen, welche Metalle oxidiert oder reduziert werden können.
Bedeutung in organischen Verbindungen
In organischen Chemie spielen Oxidationszahlen ebenfalls eine zentrale Rolle. Sie helfen uns dabei, verschiedene funktionelle Gruppen zu identifizieren und deren chemisches Verhalten vorherzusagen. Zum Beispiel:
- Ester haben typischerweise eine niedrigere Oxidationszahl als Carbonsäuren aufgrund des unterschiedlichen Wasserstoffgehalts.
- Kohlenhydrate weisen unterschiedliche Oxidationsstufen auf, abhängig davon, wie viele Hydroxylgruppen sie enthalten.
- Sauerstoff- und Stickstoffverbindungen zeigen oft komplexe Wechselwirkungen basierend auf ihren jeweiligen Oxidationszahlen.
| Molekültyp | Typische Oxidationszahl für Kohlenstoff (C) |
|---|---|
| Kohlenwasserstoffe (Alkane) | -4 bis 0 |
| Caronylverbindungen (Ketone) | =+1 bis +2 |
| Säuren (Carbonsäuren) | =+3 bis +4 |
Anwendungen in analytischen Methoden
Zudem sind Oxidationszahlen ein wesentliches Element in vielen analytischen Methoden wie der Titration oder spektroskopischen Verfahren. Bei Titrationen wird häufig das Prinzip verwendet, dass sich beim Erreichen des Äquivalenzpunkts die Oxidationszahlen, sowie deren Veränderungen nachvollziehen lassen:
- Titrationen zur Bestimmung von Reduktionsmitteln nutzen Änderungen der dynamisch ermittelten Oxidationseigenschaften .
- Spektroskopische Techniken wie UV-Vis oder NMR setzen Kenntnisse über Oxidation voraus um Strukturinformationen abzuleiten.
- Dank moderner Technologien können wir sogar mittels Computermodellierung Vorhersagen über mögliche Reaktionswege treffen basierend auf den postulierten Oxida tions zahlen .
- Zink und Kupfersulfat:
- Zn + CuSO₄ → ZnSO₄ + Cu
- Hier erhöht sich die Oxidationszahl des Zinks, während sie beim Kupfer sinkt.
- Eisen(III)-chlorid und Aluminium:
- 2Al + 3FeCl₃ → 3Fe + 2AlCl₃
- Eisen wird durch Aluminium reduziert; Al verliert Elektronen an Fe³⁺.
- In der organischen Chemie zur Bestimmung von Reaktionsmechanismen.
- In der Elektrochemie zur Analyse galvanischer Zellen.
- In biologischen Systemen zur Untersuchung redoxaktiver Enzyme.
Diese Anwendungen zeigen deutlich, dass ein fundiertes Verständnis der Oxidationszahlen nicht nur theoretisch bedeutend ist, sondern auch praktische Implikationen für verschiedene Bereiche innerhalb der Chemie hat.
Häufige Fehler bei der Bestimmung von Oxidationszahlen
Die Bestimmung von Oxidationszahlen kann manchmal eine Herausforderung darstellen, insbesondere für Studierende und Chemiker, die sich mit komplexeren Verbindungen auseinandersetzen. Einige häufige Fehler treten auf, wenn grundlegende Regeln nicht beachtet oder missverstanden werden. In diesem Abschnitt werden wir die gängigsten Irrtümer beleuchten und erläutern, wie sie vermieden werden können.
Missverständnisse bei den Regelwerken
Ein häufiger Fehler liegt im Verständnis der Regeln zur Bestimmung der Oxidationszahlen. Oft wird die Bedeutung der Elektronegativität übersehen. Wenn Atome in einer Verbindung unterschiedliche Elektronegativitäten aufweisen, sollte dies Einfluss auf ihre Oxidationszahlen haben. Beispielsweise wird Sauerstoff normalerweise als -2 betrachtet, es sei denn, er ist in Peroxiden oder Fluorverbindungen eingebunden.
Vernachlässigung von Summenregeln
Ein weiterer verbreiteter Fehler ist das Ignorieren der Summenregel für Oxidationszahlen. Die Summe der Oxidationszahlen in einer neutralen Verbindung muss gleich Null sein; in Ionen muss sie dem Ladungszustand des Ions entsprechen. Viele machen den Fehler zu glauben, dass diese Regel nicht immer gilt oder dass sie bei komplexeren Molekülen irrelevant ist.
Unklare Identifikation von Elementen
Darüber hinaus sehen wir oft ungenaue Identifikationen von Elementen innerhalb einer Verbindung. Es ist entscheidend zu erkennen, welche Atome tatsächlich an einer Reaktion beteiligt sind und deren jeweilige Oxidationsstufen korrekt zuzuordnen. So kann beispielsweise Kohlenstoff in unterschiedlichen funktionellen Gruppen sehr unterschiedliche Oxidationszahlen annehmen.
| Beispiel | Typische Oxidationszahl |
|---|---|
| Alkohole | -1 bis +1 |
| Aldehyde | +1 |
| Carbonsäuren | +3 bis +4 |
Diese Tabelle zeigt deutlich die Variabilität der Oxidationszahlen unter verschiedenen Bedingungen und Zusammensetzungen auf.
Schlussfolgerung zu häufigen Fehlern
Um diese typischen Fehler zu vermeiden, empfehlen wir eine systematische Herangehensweise: Prüfen Sie zuerst alle relevanten Regeln zur Bestimmung von Oxidationszahlen, achten Sie besonders auf Elektronegativitäten und verwenden Sie geeignete Hilfsmittel wie Tabellen zur Überprüfung Ihrer Ergebnisse. Ein gründliches Verständnis dieser Aspekte wird Ihnen helfen, präzisere Analysen durchzuführen und Ihre Kenntnisse über chemische Reaktionen weiter zu vertiefen.
Die Rolle der Oxidationszahlen in Redoxreaktionen
Die Untersuchung der Rolle von Oxidationszahlen in Redoxreaktionen ist für das Verständnis chemischer Prozesse von zentraler Bedeutung. In einer Redoxreaktion finden immer Elektronenübertragungen statt, wobei ein Element oxidiert und ein anderes reduziert wird. Die Oxidationszahlen helfen uns, diese Veränderungen nachzuvollziehen und die beteiligten Elemente zu identifizieren.
Ein grundlegendes Konzept ist, dass die Oxidation mit einem Anstieg der Oxidationszahl verbunden ist, während die Reduktion mit einem Rückgang einhergeht. Zum Beispiel in der Reaktion zwischen Zink und Kupfer(II)-sulfat:
* Zink (Zn) wird oxidiert von 0 auf +2.
* Kupfer (Cu) wird reduziert von +2 auf 0.
Um solche Reaktionen korrekt zu analysieren, müssen wir die Oxidationszahlen der einzelnen Elemente vor und nach der Reaktion bestimmen.
Beispiele für Redoxreaktionen
Hier sind einige häufige Beispiele:
Diese Beispiele verdeutlichen nicht nur den Prozess der Elektronenübertragung, sondern auch wie wichtig es ist, die korrekten Oxidationszahlen zu kennen, um den Verlauf jeder Reaktion verstehen zu können.
Bedeutung in verschiedenen Bereichen
Die Anwendung von Oxidationszahlen erstreckt sich über verschiedene chemische Disziplinen:
Das Verständnis dieser Konzepte ermöglicht es uns nicht nur, chemische Gleichungen auszugleichen, sondern auch tiefere Einblicke in Stoffwechselprozesse oder industrielle Anwendungen zu gewinnen. So tragen die Oxidationszahlen entscheidend dazu bei, unser Wissen über chemische Interaktionen umfassend zu erweitern.