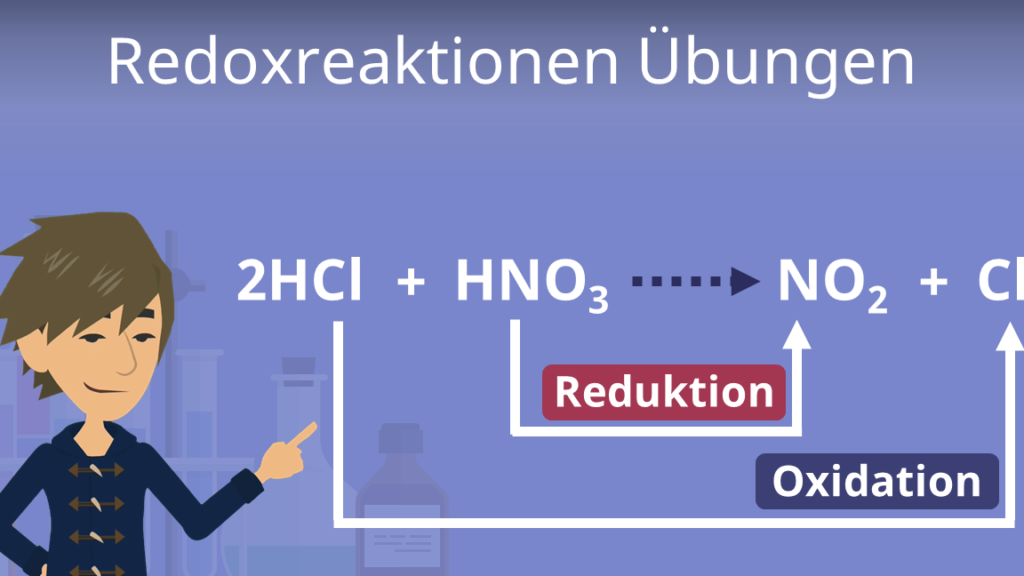
Redoxreaktionen sind ein zentrales Thema in der Chemie und spielen eine entscheidende Rolle in vielen chemischen Prozessen. Durch das Verständnis von Redoxreaktionen können wir tiefere Einblicke in die Funktionsweise von Batterien, Korrosion und sogar biologischen Systemen gewinnen. In unserem Artikel widmen wir uns den wichtigsten Aspekten der redoxreaktion übungen für Studenten und Schüler.
Wir bieten eine Vielzahl von Übungen an, die nicht nur das theoretische Wissen vertiefen, sondern auch praktische Fähigkeiten fördern. Praktische Anwendungen und Beispiele helfen uns, die Konzepte besser zu verstehen und anzuwenden. Welche Herausforderungen begegnen uns bei der Lösung dieser Aufgaben? Lassen Sie sich inspirieren und entdecken Sie mit uns die faszinierende Welt der Redoxreaktionen!
Redoxreaktion Übungen für Anfänger und Fortgeschrittene
Um das Verständnis von Redoxreaktionen zu vertiefen, ist es wichtig, sowohl für Anfänger als auch für Fortgeschrittene geeignete Übungen bereitzustellen. Diese Übungen helfen nicht nur dabei, die grundlegenden Konzepte zu festigen, sondern fördern auch das analytische Denken und die Problemlösungsfähigkeiten im Bereich der Chemie.
Übungen für Anfänger
Für diejenigen, die neu in der Welt der Redoxreaktionen sind, bieten sich einfache Aufgaben an:
- Identifikation von Oxidations- und Reduktionsmitteln:
- Gegeben sei die Reaktion: ( text{Zn} + text{Cu}^{2+} rightarrow text{Zn}^{2+} + text{Cu} ).
- Bestimmen Sie das Oxidationsmittel und das Reduktionsmittel.
- Oxidationszahlen ermitteln:
- Berechnen Sie die Oxidationszahlen in den folgenden Verbindungen:
- ( text{H}_2text{O} )
- ( text{NaCl} )
- ( text{SO}_4^{2-} )
- Balancieren einfacher Redoxreaktionen:
- Balancieren Sie folgende Reaktion im sauren Medium:
- ( text{MnO}_4^- + 5text{Fe}^{2+} + 8text{H}^+ → text{Mn}^{2+} + 5text{Fe}^{3+} + 4text{H}_2text{O} ).
Übungen für Fortgeschrittene
Fortgeschrittene Studierende sollten sich komplexeren Aufgaben stellen:
- Komplexere Reaktionen analysieren:
- Betrachten Sie die Reaktion zwischen Wasserstoffperoxid und Iodidionen:
- Stellen Sie eine vollständige Gleichung auf und bestimmen Sie alle Oxidationszahlen.
- Energiebilanzen berechnen:
- Berechnen Sie die Gibbs-Energieänderung (( ΔG°_r )) einer gegebenen Redoxreaktion unter Standardbedingungen.
- Anwendungen von Redoxreaktionen in der Industrie:
- Diskutieren Sie reale Anwendungen von Redoxreaktionen z.B., wie sie in Batterien oder bei elektrochemischen Prozessen verwendet werden.
Diese gezielten Redoxreaktion Übungen sind entscheidend dafür, dass wir ein tiefes Verständnis dieser chemischen Prozesse entwickeln können. Indem wir uns sowohl mit grundlegenden als auch fortgeschrittenen Themen beschäftigen, stärken wir unser Wissen und unsere Fähigkeiten kontinuierlich.
Wichtige Konzepte der Redoxreaktionen verstehen
Um die zugrunde liegenden Mechanismen von Redoxreaktionen zu durchdringen, müssen wir einige wichtige Konzepte verstehen. Diese Konzepte sind entscheidend für das korrekte Lösen von Aufgaben und das Verstehen der chemischen Prozesse, die in diesen Reaktionen ablaufen.
Ein zentrales Element ist die Oxidationszahl, die den Grad der Oxidation eines Atoms in einer Verbindung angibt. Sie hilft uns dabei zu erkennen, wie Elektronen zwischen Atomen transferiert werden. In einer Redoxreaktion gibt es immer ein Oxidationsmittel, das Elektronen aufnimmt, und ein Reduktionsmittel, das Elektronen abgibt. Das Verständnis dieser Begriffe ist fundamental.
Die Rolle von Oxidation und Reduktion
Jede Redoxreaktion umfasst zwei Teilprozesse: Oxidation und Reduktion. Bei der Oxidation verliert ein Atom oder Ion Elektronen, während bei der Reduktion Elektronen gewonnen werden. Um dies zu verdeutlichen, betrachten wir folgendes Beispiel:
- In der Reaktion ( text{2Cu} + text{O}_2 rightarrow text{2CuO} ) wird Kupfer oxidiert (es verliert Elektronen) und Sauerstoff wird reduziert (es gewinnt Elektronen).
Anwendung des Konzeptes
Das Verständnis dieser grundlegenden Konzepte ermöglicht es uns nicht nur, einfache Gleichungen zu lösen, sondern auch komplexere Systeme zu analysieren. Wir können zum Beispiel erkennen, dass in vielen biologischen Prozessen wie der Zellatmung ähnliche Prinzipien gelten.
Zusätzlich sollten wir beachten:
- Der pH-Wert kann einen erheblichen Einfluss auf den Verlauf von Redoxreaktionen haben.
- Die Temperatur kann ebenfalls eine Rolle spielen; höhere Temperaturen erhöhen oft die Reaktionsgeschwindigkeit.
Indem wir diese wichtigen Konzepte im Hinterkopf behalten und sie aktiv in unseren Übungen zur Redoxreaktion anwenden, können wir unser Wissen vertiefen und unsere Fähigkeiten verbessern.
Praktische Beispiele zur Anwendung von Redoxreaktionen
Um die Konzepte von Redoxreaktionen weiter zu veranschaulichen, sollten wir praktische Beispiele betrachten, die in verschiedenen Bereichen der Chemie Anwendung finden. Diese Beispiele helfen uns nicht nur dabei, das theoretische Wissen anzuwenden, sondern auch reale chemische Prozesse besser zu verstehen. Hier sind einige relevante Anwendungen:
Beispiel 1: Batterien
Batterien sind hervorragende Beispiele für Redoxreaktionen im Alltag. In einer Lithium-Ionen-Batterie findet eine Oxidation und Reduktion statt, wenn die Batterie entladen oder geladen wird. Während des Entladevorgangs oxidiert Lithium und gibt Elektronen ab, während ein anderes Material reduziert wird und Elektronen aufnimmt.
| Prozess | Oxidation | Reduktion |
|---|---|---|
| Entladung | ( text{Li}^+ + e^- rightarrow text{Li} ) | ( text{CoO}2 + e^- rightarrow text{CoO}_2^- ) |
| Ladung | ( text{Li} rightarrow text{Li}^+ + e^- ) | ( text{CoO}_2^- + e^- rightarrow text{CoO}_2) |
Beispiel 2: Korrosion
Korrosion ist ein weiteres praktisches Beispiel, das wir untersuchen können. Bei der Korrosion von Eisen handelt es sich um eine schleichende Oxidationsreaktion, bei der Eisen mit Sauerstoff reagiert und rostet. Dies geschieht in Anwesenheit von Wasser:
[
text{4Fe} + 3text{O}_2 + 6text{H}_2text{O} → 4text{Fe(OH)}_3
]
Hierbei wird Eisen oxidiert (es verliert Elektronen), während Sauerstoff reduziert wird (es gewinnt Elektronen).
Beispiel 3: Biochemische Prozesse
In biologischen Systemen spielen Redoxreaktionen eine entscheidende Rolle. Ein bekanntes Beispiel ist die Zellatmung, bei der Glucose oxidiert wird und Sauerstoff reduziert wird:
[
text{C}_6text{H}{12}text{O}_6 + 6text{O}_2 → 6text{CO}_2 + 6text{H}_2text{O}
]
Diese Reaktion ist essentiell für das Leben und zeigt deutlich die Bedeutung von Redoxreaktionen in biologischen Prozessen.
Durch diese praktischen Beispiele zur Anwendung von Redoxreaktionen erkennen wir den Einfluss dieser chemischen Prozesse auf verschiedene Lebensbereiche – sei es in Technologie oder Naturwissenschaften. Indem wir uns mit diesen Beispielen auseinandersetzen und sie in unseren Übungen zur redoxreaktion übungen berücksichtigen, vertiefen wir unser Verständnis erheblich.
Tipps zur Lösung von Redoxgleichungen
Um Redoxgleichungen erfolgreich zu lösen, ist es entscheidend, einige grundlegende Tipps und Strategien zu beachten. Diese können uns dabei helfen, die Schritte zur Identifizierung von Oxidations- und Reduktionsprozessen klarer zu verstehen und anzuwenden. Hier sind einige wertvolle Hinweise:
- Identifizieren Sie die Oxidationszahlen: Beginnen wir damit, die Oxidationszahlen der Elemente in der Reaktion festzulegen. Dies ermöglicht es uns, schnell herauszufinden, welche Elemente oxidiert (Elektronen verlieren) und welche reduziert (Elektronen gewinnen) werden.
- Trennen Sie die Teilreaktionen: Es ist hilfreich, die gesamte Reaktion in zwei separate Teilreaktionen aufzuteilen – eine für die Oxidation und eine für die Reduktion. Dadurch wird der Überblick über den Elektronentransfer einfacher.
- Gleichgewicht der Elektronen: Achten wir darauf, dass die Anzahl der Elektronen, die bei der Oxidation verloren gehen, gleich der Anzahl der Elektronen ist, die bei der Reduktion gewonnen werden. Falls nötig, fügen wir Koeffizienten hinzu, um dies sicherzustellen.
- Berücksichtigen Sie saure oder alkalische Bedingungen: Bestimmen wir den pH-Wert des Mediums; das beeinflusst möglicherweise unsere Herangehensweise an den Ausgleich von Wasserstoff- und Hydroxidionen in den Gleichungen.
- Prüfen Sie Ihre Ergebnisse: Nachdem wir alle Schritte abgeschlossen haben, sollten wir überprüfen, ob sowohl Masse als auch Ladung auf beiden Seiten der Gleichung ausgeglichen sind.
Beispiel zur Veranschaulichung
Nehmen wir als Beispiel folgende Reaktion:
[ text{Zn} + text{Cu}^{2+} → text{Zn}^{2+} + text{Cu} ]
- Zuerst bestimmen wir die Oxidationszahlen:
- Zn: 0 (Elementarform) → Zn²⁺: +2 (oxidiert)
- Cu²⁺: +2 → Cu: 0 (reduziert)
- Die Teilreaktionen wären:
- Oxidation: ( text{Zn} → text{Zn}^{2+} + 2e^- )
- Reduktion: ( text{Cu}^{2+} + 2e^- → text{Cu} )
Durch diese strukturierte Vorgehensweise verbessern wir unser Verständnis von Redoxreaktionen erheblich und erleichtern uns das Lösen entsprechender Aufgaben in unseren Übungen zur redoxreaktion übungen.
Häufige Fehler bei Redoxreaktionen vermeiden
Bei der Bearbeitung von Redoxreaktionen ist es wichtig, häufige Fehler zu vermeiden, um die Ergebnisse unserer Übungen zur redoxreaktion übungen korrekt und zuverlässig zu gestalten. Trotz des klaren Verfahrens kann es leicht passieren, dass wir in bestimmte Fallen tappen. Hier sind einige der häufigsten Fehler sowie Tipps, wie wir sie umgehen können:
Unzureichende Identifikation der Oxidationszahlen
Ein häufiger Fehler besteht darin, die Oxidationszahlen nicht richtig zu bestimmen oder gar ganz zu ignorieren. Dies kann dazu führen, dass wir den Oxidations- und Reduktionsprozess falsch einschätzen. Um dies zu vermeiden, sollten wir stets systematisch vorgehen und jede Verbindung sorgfältig analysieren.
Ungleichgewicht bei Elektronenübertragungen
Ein weiterer verbreiteter Fehler ist das Missverhältnis zwischen den Elektronen, die bei der Oxidation verloren gehen und denen, die bei der Reduktion gewonnen werden. Es ist entscheidend sicherzustellen, dass beide Seiten gleich viele Elektronen beinhalten. Falls nötig, müssen wir Koeffizienten anpassen oder zusätzliche Schritte einfügen.
Vernachlässigung von Bedingungen
Die Berücksichtigung des pH-Werts wird oft übersehen. Ob in sauren oder alkalischen Lösungen gearbeitet wird, beeinflusst unsere Gleichungen erheblich. Falsche Annahmen über den Zustand des Mediums können falsche Ergebnisse liefern.
Mangelnde Überprüfung der Endergebnisse
Schließlich neigen wir manchmal dazu, unsere Ergebnisse nicht gründlich genug zu überprüfen. Sowohl Masse als auch Ladung müssen auf beiden Seiten ausgeglichen sein; andernfalls könnte das Ergebnis ungenau sein. Eine genaue Kontrolle nach Abschluss jeder Übung hilft uns dabei, diese typischen Fehler auszuschließen.
Indem wir uns dieser häufigen Probleme bewusst sind und entsprechende Maßnahmen ergreifen, verbessern wir unser Verständnis für Redoxreaktionen erheblich und erhöhen die Genauigkeit unserer Arbeiten in den redoxreaktion übungen.