Die Säure-Base-Reaktion ist ein grundlegendes Konzept in der Chemie, das nicht nur für Wissenschaftler von Bedeutung ist, sondern auch für unser tägliches Leben. Diese Reaktionen sind entscheidend für zahlreiche Prozesse, die von der Verdauung in unserem Körper bis hin zur Herstellung von Alltagsprodukten reichen. In diesem Artikel werden wir die Grundlagen der Säure-Base-Reaktion erläutern und einige anschauliche Beispiele vorstellen.
Unser Ziel ist es, ein besseres Verständnis dafür zu entwickeln, wie Säuren und Basen miteinander interagieren. Wir werden erkunden, was eine Säure-Base-Reaktion ausmacht und warum sie so wichtig ist. Welche Rolle spielen pH-Werte dabei? Und wie beeinflussen diese Reaktionen unsere Umwelt? Lassen Sie uns gemeinsam eintauchen in die faszinierende Welt der chemischen Wechselwirkungen und herausfinden, warum dieses Thema für jeden von uns relevant sein kann.
Säure-Base-Reaktion im Chemieunterricht verstehen
Im Chemieunterricht ist das Verständnis von Säure-Base-Reaktionen entscheidend, da sie in vielen wissenschaftlichen Disziplinen eine zentrale Rolle spielen. Diese Reaktionen sind nicht nur theoretisch wichtig, sondern auch praktisch relevant für zahlreiche alltägliche Anwendungen. Durch die Vermittlung der grundlegenden Prinzipien können wir Schülern helfen, ein tieferes Verständnis für chemische Prozesse zu entwickeln.
Ein Aspekt, den wir besonders hervorheben sollten, ist die Bedeutung der Reaktionsgleichungen. Diese Gleichungen ermöglichen es uns, die Veränderungen während einer Säure-Base-Reaktion präzise darzustellen und zu analysieren. Ein Beispiel hierfür ist die Neutralisation zwischen einer Säure und einer Base:
- Säuren geben Protonen (H⁺) ab.
- Basen nehmen Protonen auf.
- Die Reaktion resultiert in Wasser und einem Salz.
Um diese Konzepte klarer zu machen, verwenden wir oft Modelle oder Diagramme im Unterricht, um visuelle Hilfen bereitzustellen.
Didaktische Ansätze
Um das Thema anschaulich zu vermitteln, setzen wir verschiedene didaktische Methoden ein:
- Experimente: Praktische Versuche fördern das Verständnis durch eigene Erfahrungen.
- Visualisierungen: Diagramme und Illustrationen zeigen den Verlauf von Reaktionen.
- Diskussionen: Gruppenarbeiten regen zum Austausch über Konzepte an und vertiefen das Wissen.
Verbindungen zu anderen Themen
Das Lernen über Säure-Base-Reaktionen eröffnet zudem Verknüpfungen zu anderen chemischen Konzepten wie dem pH-Wert oder der Brønsted-Lowry-Theorie. Diese Zusammenhänge verstärken das ganzheitliche Verständnis der Chemie bei unseren Schülern und ermutigen sie dazu, kritisch über chemische Phänomene nachzudenken.
Mit diesen Ansätzen möchten wir sicherstellen, dass unsere Schüler nicht nur lernen, sondern auch verstehen können, wie wichtig die Kenntnisse über Säure-Base-Reaktionen in der realen Welt sind.
Die Rolle von Protonen in Säure-Base-Reaktionen
Protonen spielen eine zentrale Rolle in Säure-Base-Reaktionen, da sie die Hauptakteure sind, die den Austausch zwischen Säuren und Basen ermöglichen. In diesen Reaktionen gibt eine Säure Protonen (H⁺) ab, während eine Base diese Protonen aufnimmt. Dieser Prozess führt zu einer Vielzahl von Veränderungen in der chemischen Zusammensetzung der Reaktionspartner und ist entscheidend für das Verständnis der zugrunde liegenden Mechanismen.
Ein wichtiges Konzept ist die Brønsted-Lowry-Theorie, die besagt, dass jede Substanz als Säure oder Base fungieren kann, abhängig davon, ob sie Protonen abgibt oder aufnimmt. Um dies zu verdeutlichen, betrachten wir einige Schlüsselmerkmale dieser Theorie:
- Säuren: Definiert als Stoffe, die Protonen abgeben können.
- Basen: Definiert als Stoffe, die Protonen aufnehmen können.
- Konjugierte Paare: Jede Säure hat ein konjugiertes Base-Paar und umgekehrt; diese Paare sind direkt miteinander verbunden durch den Verlust oder Gewinn eines Protons.
Die Fähigkeit von Molekülen, Protonen zu übertragen, beeinflusst nicht nur ihre chemischen Eigenschaften sondern auch ihre Reaktivität. Beispielsweise kann Wasser sowohl als Säure (wenn es ein Proton abgibt) als auch als Base (wenn es ein Proton aufnimmt) agieren. Dies macht Wasser zu einem einzigartigen Lösungsmittel in vielen chemischen Reaktionen.
In praktischen Anwendungen zeigt sich dies deutlich in alltäglichen Prozessen wie der Verdauung oder der Herstellung von Düngemitteln und Medikamenten. Die Beherrschung dieser Konzepte hilft uns nicht nur im Unterricht weiterzukommen; sie ermöglicht uns auch einen tieferen Einblick in zahlreiche industrielle Verfahren und biologische Systeme.
Um unseren Schülern das Verständnis für diese komplexe Materie zu erleichtern, verwenden wir oft Modelle zur Veranschaulichung des Protonentransfers bei verschiedenen Säure-Base-Reaktionen. Diese visuellen Hilfen fördern ein intuitives Verständnis dessen, was theoretisch oft schwierig nachvollziehbar scheint.
Beispiele für alltägliche Säure-Base-Reaktionen
In unserem täglichen Leben begegnen wir zahlreichen Beispielen für Säure-Base-Reaktionen, die oft unbemerkt bleiben, aber entscheidend für viele chemische Vorgänge sind. Diese Reaktionen finden in verschiedenen Kontexten statt, von der Küche über die Natur bis hin zu industriellen Anwendungen. Indem wir uns mit diesen alltäglichen Prozessen beschäftigen, können wir ein tieferes Verständnis für die Rolle von Säuren und Basen in unserer Umwelt entwickeln.
1. Verdauung im menschlichen Körper
Ein klassisches Beispiel ist die Verdauung, bei der Magensäure (hauptsächlich Salzsäure) eine Schlüsselrolle spielt. Diese Säure hilft nicht nur beim Abbau von Nahrungsmitteln, sondern aktiviert auch Enzyme wie Pepsin. Hierbei gibt die Magensäure Protonen ab, während andere Moleküle als Basen fungieren und diese Protonen aufnehmen:
- Magensäure: HCl → Protone werden abgegeben.
- Bicarbonat aus dem Pankreas: HCO₃⁻ + H⁺ → Neutralisation.
Dieser Prozess ist unerlässlich für eine effektive Verdauung und zeigt deutlich den Einfluss von Säuren und Basen auf biologische Systeme.
2. Backen mit Natron
Ein weiteres anschauliches Beispiel findet sich beim Backen: Die Verwendung von Natron (Natriumbicarbonat) zusammen mit einer Säure wie Essig oder Zitronensaft führt zu einer spannenden Säure-Base-Reaktion. Wenn diese beiden Zutaten gemischt werden, entsteht Kohlendioxidgas (CO₂), das den Teig auflockert:
- Reaktionsgleichung: NaHCO₃ + CH₃COOH → CO₂ + H₂O + NaCH₃COO
Diese Reaktion ist entscheidend dafür, dass beispielsweise Kuchen luftig und leicht werden.
3. Reinigung mit Essig
Essig wird häufig als umweltfreundliches Reinigungsmittel eingesetzt. In diesem Kontext zeigt sich die Wirksamkeit seiner sauren Eigenschaften besonders gut bei der Entfernung von Kalkablagerungen:
- Reaktion mit Kalziumkarbonat: CaCO₃ (Kalk) reagiert mit Essigsäure (CH₃COOH), was zur Bildung von Wasser, Kohlenstoffdioxid und Calciumacetat führt:
| Reaktanten | Produkte |
|---|---|
| CaCO₃ + CH₃COOH | H₂O + CO₂ + Ca(CH₃COO)₂ |
Durch diese einfache chemische Reaktion kann Kalk effektiv entfernt werden, was die Anwendung im Haushalt vereinfachte.
Diese Beispiele verdeutlichen eindrucksvoll, wie tief verwurzelt Säure-Base-Reaktionen in unserem Alltag sind und welche wichtigen Funktionen sie erfüllen – sei es in biologischen Prozessen oder praktischen Anwendungen in unserem täglichen Leben.
Der pH-Wert und seine Bedeutung für die Reaktionsdynamik
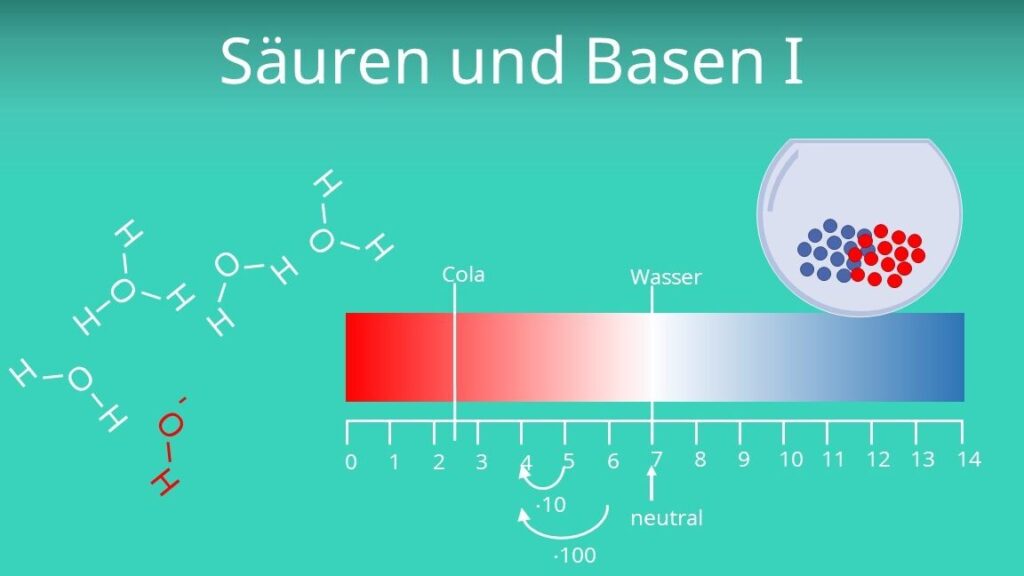
Der pH-Wert ist ein entscheidender Faktor, wenn es um die Dynamik von Säure-Base-Reaktionen geht. Er gibt an, wie sauer oder basisch eine Lösung ist und beeinflusst somit direkt die Geschwindigkeit und das Gleichgewicht chemischer Reaktionen. In der Chemie wird der pH-Wert auf einer Skala von 0 bis 14 gemessen, wobei Werte unter 7 als sauer, Werte von 7 als neutral und Werte über 7 als basisch gelten. Diese Klassifizierung hat weitreichende Implikationen für verschiedene chemische Prozesse.
Ein wichtiger Aspekt des pH-Wertes ist seine Auswirkung auf die Verfügbarkeit von Protonen (H⁺). Je niedriger der pH-Wert, desto mehr Protonen sind in der Lösung vorhanden. Dies kann die Reaktionsgeschwindigkeit erhöhen, da viele Säure-Base-Reaktionen durch den Transfer von Protonen charakterisiert sind. Umgekehrt bedeutet ein hoher pH-Wert weniger verfügbare Protonen und kann zu einer verlangsamten Reaktion führen.
Einfluss auf biochemische Prozesse
In biologischen Systemen spielt der pH-Wert eine ebenso bedeutende Rolle für enzymatische Aktivitäten und Stoffwechselprozesse. Enzyme haben spezifische pH-Bereiche, in denen sie optimal arbeiten können. Abweichungen vom idealen pH-Bereich können nicht nur die Aktivität dieser Enzyme beeinträchtigen, sondern auch ihre Struktur verändern:
- Enzymaktivität: Ein Beispiel ist das Enzym Pepsin im Magen, das bei einem sauren pH optimal arbeitet.
- Stabilität von Molekülen: Oberhalb eines bestimmten pH-Wertes können Proteine denaturieren.
Anwendungen in der Industrie
Die Kontrolle des pH-Wertes ist auch in industriellen Prozessen unerlässlich. Bei vielen chemischen Reaktionen müssen bestimmte Bedingungen eingehalten werden, um optimale Ergebnisse zu erzielen:
| Anwendung | Optimaler pH-Bereich |
|---|---|
| Lebensmittelverarbeitung | 4 – 6 |
| Wasseraufbereitung | 6 – 8 |
| Pharmazeutische Produktion | variabel |
Zusammenfassend lässt sich sagen, dass der pH-Wert nicht nur eine grundlegende Eigenschaft jeder Lösung darstellt, sondern auch einen wesentlichen Einfluss auf die gesamte Reaktionsdynamik hat. Das Verständnis dieses Zusammenhangs ermöglicht uns eine bessere Steuerung und Optimierung vielfältiger chemischer Prozesse in unserem Alltag sowie in industriellen Anwendungen.
Wichtige Konzepte der Brønsted-Lowry-Theorie
Die Brønsted-Lowry-Theorie ist ein fundamentales Konzept in der Chemie, das hilft, die Dynamik von Säure-Base-Reaktionen zu verstehen. Nach dieser Theorie werden Säuren als Protonendonatoren und Basen als Protonenakzeptoren definiert. Diese Definition erweitert unser Verständnis von chemischen Reaktionen über die traditionelle Sichtweise hinaus und ermöglicht uns, eine Vielzahl von Reaktionen zu klassifizieren.
Ein zentrales Element dieser Theorie ist der Protonentransfer, der das Herzstück der meisten Säure-Base-Reaktionen bildet. Wenn eine Säure ein Proton abgibt, entsteht gleichzeitig eine konjugierte Base. Umgekehrt kann die Aufnahme eines Protons durch eine Base zur Bildung einer konjugierten Säure führen. Dieser Prozess stellt sicher, dass jede Säure und ihre korrespondierende Base in einem dynamischen Gleichgewicht stehen.
Die Rolle von konjugierten Paaren
In der Brønsted-Lowry-Theorie sind konjugierte Paare entscheidend für das Verständnis der Wechselwirkungen zwischen verschiedenen Substanzen während einer säure-base reaktion. Ein konjugiertes Paar besteht aus einer Säure und ihrer entsprechenden Base oder umgekehrt:
- Beispiel: HCl (Säure) und Cl⁻ (konjugierte Base)
- Beispiel: NH₄⁺ (konjugierte Säure) und NH₃ (Base)
Diese Paare zeigen auf, wie leicht eine Verbindung Protonen abgeben oder aufnehmen kann, was direkt mit ihrer Stärke als Säuren oder Basen zusammenhängt.
Starke und schwache Säuren sowie Basen
Die Brønsted-Lowry-Theorie unterscheidet auch zwischen starken und schwachen Säuren sowie Basen basierend auf ihrer Fähigkeit zur Protonenspende oder -aufnahme:
- Starke Säuren geben fast vollständig ihre Protonen ab; ein Beispiel ist Salzsäure (HCl).
- Schwache Säuren dissoziieren nur teilweise; dazu gehört Essigsäure (CH₃COOH).
Ähnlich verhält es sich bei den Basen:
- Starke Basen, wie Natriumhydroxid (NaOH), nehmen schnell Protonen auf.
- Schwache Basen, wie Ammoniak (NH₃), zeigen diese Eigenschaft nur begrenzter.
Das Verständnis dieser Konzepte ist essenziell für die Analyse von chemischen Reaktionen in unterschiedlichen Kontexten, einschließlich industrieller Anwendungen und biologischer Prozesse.