Salze sind faszinierende chemische Verbindungen, die in vielen Bereichen unseres Lebens eine Rolle spielen. Wusstet ihr, dass Salze nicht nur in der Küche, sondern auch in der Industrie und in der Natur vorkommen? In diesem Artikel werfen wir einen Blick auf die wichtigsten Salze und ihre Eigenschaften.
Unsere umfassende Salze Chemie Liste bietet eine Übersicht über die gängigsten Salze, ihre Formeln und Anwendungen. Von Natriumchlorid bis zu Calciumcarbonat – jedes Salz hat seine eigenen einzigartigen Merkmale und Funktionen.
Lasst uns gemeinsam die Welt der Salze erkunden und herausfinden, wie sie unsere Umwelt und Technologie beeinflussen. Seid ihr bereit, mehr über diese spannenden chemischen Verbindungen zu erfahren?
Was Sind Salze In Der Chemie?
Salze sind chemische Verbindungen, die aus Kationen und Anionen bestehen. Sie spielen eine fundamentale Rolle in vielen chemischen Prozessen und kommen in der Natur und im Alltag häufig vor.
Salze entstehen durch die Reaktion von Säuren mit Basen. Diese Reaktionen sind essenziell für zahlreiche biologische und industrielle Abläufe. Auch in der Umwelt spielen Salze eine wesentliche Rolle, beispielsweise im Wasserhaushalt von Organismen.
Typische Eigenschaften von Salzen sind:
Salze sind in verschiedenen Anwendungen zu finden. Hier einige Beispiele:
Die chemische Formel stellt eine ausreichende Beschreibung von Salzen zur Verfügung. Einige häufige Salze und ihre Namen umfassen:
| Salz | Chemische Formel |
|---|---|
| Natriumchlorid | NaCl |
| Kaliumsulfat | K₂SO₄ |
| Calciumcarbonat | CaCO₃ |
Salze sind auch entscheidend für physiologische Prozesse. Sie helfen bei der Aufrechterhaltung des Elektrolytgleichgewichts im menschlichen Körper. Darüber hinaus sind Salze für viele biochemische Reaktionen unentbehrlich.
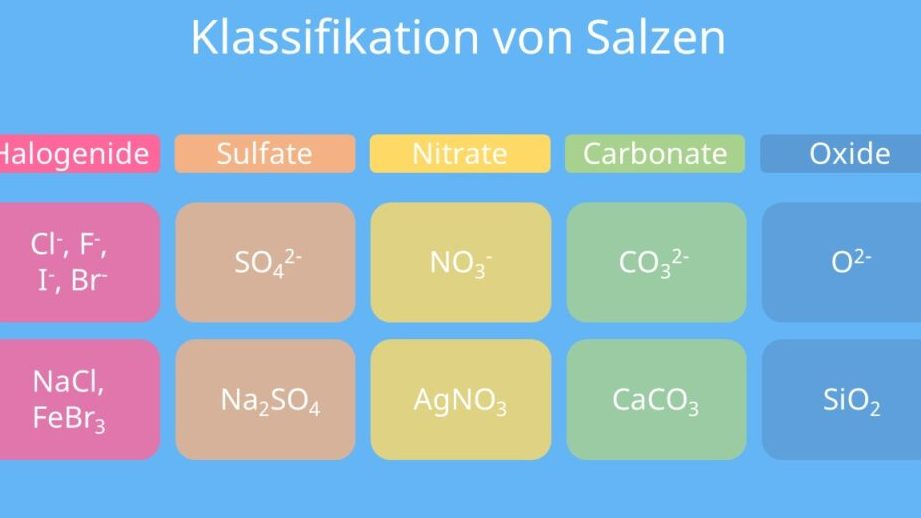
Salze lassen sich in verschiedene Kategorien einteilen, wie:
Insgesamt sind Salze vielseitige Verbindungen, deren Verständnis wesentlich für Chemie, Biologie und Industrie ist.
Wichtige Eigenschaften Von Salzen
Salze besitzen charakteristische Merkmale, die in vielen Anwendungen zentral sind. Sie zeigen eine Vielzahl von Eigenschaften, die deren Funktionalität in Wissenschaft und Industrie beeinflussen.
Löslichkeit
Die Löslichkeit von Salzen in Wasser variiert erheblich. Einige Salze sind stark löslich, während andere kaum in Wasser gelöst werden. Die Löslichkeit hängt von verschiedenen Faktoren ab, wie Temperatur und Art des Salzes. Wichtige Punkte sind:
- NaCl (Kochsalz): Sehr gut in Wasser löslich.
- AgCl (Silberchlorid): Kaum löslich in Wasser.
- K2SO4 (Kaliumsulfat): Gut löslich, vor allem bei höheren Temperaturen.
- Ba(OH)2 (Bariumhydroxid): Löslich, besonders in heißem Wasser.
Die Löslichkeit beeinflusst die Verwendung von Salzen in verschiedenen Bereichen, wie der chemischen Industrie oder der Lebensmittelverarbeitung.
Kristallstruktur
Die Kristallstruktur von Salzen ist für deren physikalische Eigenschaften bedeutend. Salze bilden meist geordnete, regelmäßige Kristallgitter. Häufige Strukturen sind:
- Ionische Gitter: Salze wie NaCl und KBr bilden kubische Kristalle.
- Hexagonale Gitter: Salze wie ZnS (Zinksulfid) weisen eine sechseckige Struktur auf.
- Orthorhombische Gitter: Beispiele sind NaNO3 (Natriumnitrat) und KNO3 (Kaliumnitrat).
- Tetragonale Gitter: CaCO3 (Calciumcarbonat) kommt in dieser Struktur vor.
Diese Strukturen beeinflussen Eigenschaften wie Schmelzpunkt, Härte und Stabilität. Deswegen sind sie entscheidend für die Auswahl von Salzen in praktischen Anwendungen.
Häufige Salze In Der Chemie
Salze spielen eine Schlüsselrolle in der Chemie und kommen in verschiedenen Anwendungen vor. Hier sind einige häufige Salze, die wir häufig antreffen.
Natriumchlorid
Natriumchlorid, allgemein als Kochsalz bekannt, ist eines der am häufigsten verwendeten Salze. Es hat verschiedene Eigenschaften und Anwendungen, darunter:
Natriumchlorid ist auch wichtig für die Aufrechterhaltung des Elektrolytgleichgewichts im menschlichen Körper. Doch, wusstest du, dass es auch in der Industrie für die Herstellung von Chlor und Natronlauge verwendet wird?
Kalziumkarbonat
Kalziumkarbonat ist ein vielseitiges Salz mit zahlreichen Anwendungen in verschiedenen Industrien. Über die wichtigsten Aspekte dieses Salzes sprechen wir jetzt:
Kalziumkarbonat ist entscheidend für die Herstellung von Zement und spielt eine wichtige Rolle in biologischen Systemen, z.B. als Bestandteil von Schalen von Meerestieren.
Magnesiumsulfat
Magnesiumsulfat, bekannt als Bittersalz, wird für verschiedene Zwecke eingesetzt. Hier sind einige Informationen zu diesem praktischen Salz:
Magnesiumsulfat hat auch eine wichtige Rolle in der Landwirtschaft, da es das Wachstum von Pflanzen fördert. Warum ist das entscheidend? Weil Pflanzen Magnesium für die Photosynthese benötigen.
Anwendungen Von Salzen
Salze finden in vielen Bereichen bedeutende Anwendungen. Diese reichen von industriellen Prozessen über den Lebensmittelsektor bis hin zu medizinischen Anwendungen.
In Der Industrie
In der Industrie spielen Salze eine entscheidende Rolle. Sie werden oft für verschiedene Zwecke eingesetzt, einschließlich:
In Der Lebensmittelindustrie
In der Lebensmittelindustrie sind Salze unverzichtbar. Einige der gängigsten Anwendungen sind:
In Der Pharmazie
Fazit
Salze sind nicht nur grundlegende chemische Verbindungen sondern auch unverzichtbare Bestandteile in vielen Lebensbereichen. Ihre einzigartigen Eigenschaften und vielfältigen Anwendungen machen sie zu einem spannenden Thema für alle, die sich mit Chemie und deren Einfluss auf unser Leben beschäftigen.
Wir haben die Bedeutung von Salzen in der Küche, der Industrie und der Natur beleuchtet und ihre Rolle in biologischen Prozessen hervorgehoben. Die verschiedenen Kategorien und Eigenschaften der Salze zeigen, wie wichtig ein fundiertes Verständnis für ihre Verwendung ist.
Durch das Wissen über Salze können wir deren Potenzial in verschiedenen Anwendungen besser ausschöpfen und verantwortungsvoll mit ihnen umgehen.