In der Welt der Chemie spielt die unpolare Atombindung eine entscheidende Rolle bei der Bildung von Molekülen. Diese Art der Bindung entsteht, wenn zwei Atome mit ähnlicher Elektronegativität aneinander gebunden sind. In diesem Artikel werden wir die wichtigsten Eigenschaften und Beispiele dieser faszinierenden Bindungsart erläutern und aufzeigen, warum sie für chemische Reaktionen von Bedeutung ist.
Wir werden uns eingehend mit den Merkmalen der unpolaren Atombindung befassen und deren Einfluss auf die physikalischen Eigenschaften von Stoffen untersuchen. Wie beeinflusst diese Bindungsart die Stabilität und Reaktivität von Molekülen? Und welche alltäglichen Beispiele finden sich in unserer Umgebung? Gemeinsam werden wir diese Fragen klären und ein tieferes Verständnis für unpolare Atombindungen entwickeln.
Eigenschaften der Unpolaren Atombindung
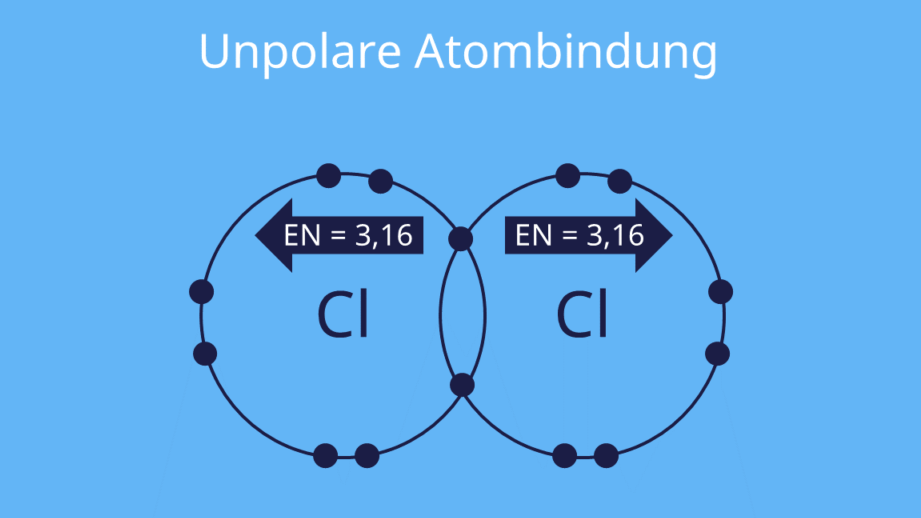
Die unpolare Atombindung zeichnet sich durch eine gleichmäßige Verteilung der Elektronen zwischen den beteiligten Atomen aus. Dies bedeutet, dass die Elektronegativität der bindenden Atome nahezu identisch ist oder sehr nahe beieinander liegt. In solchen Bindungen kommt es nicht zu einer signifikanten Verschiebung der Elektronendichte, was eine homogene Verteilung in der Molekülstruktur zur Folge hat. Diese Eigenschaften führen zu speziellen physikalischen und chemischen Merkmalen unpolarer Bindungen.
Merkmale unpolarer Atombindungen
- Geringe Polarität: Da die Elektronendichte gleichmäßig verteilt ist, zeigen unpolare Atombindungen keine signifikante Polarisierung.
- Löslichkeit: Moleküle mit unpolaren Atombindungen sind oft in unpolaren Lösungsmitteln löslich, während sie in polaren Lösungsmitteln schlecht löslich sind.
- Schmelz- und Siedepunkte: Unpolare Substanzen haben tendenziell niedrigere Schmelz- und Siedepunkte im Vergleich zu polaren Substanzen aufgrund schwächerer intermolekularer Kräfte wie Van-der-Waals-Kräfte.
Beispiele für Eigenschaften
Ein praktisches Beispiel für die finden wir in Gasen wie Stickstoff (N₂) oder Sauerstoff (O₂). Beide Gase bestehen aus zwei identischen Atomen, was zu einer starken unpolaren Bindung führt:
| Gas | Formel | Schmelzpunkt | Siedepunkt |
|---|---|---|---|
| Stickstoff | N₂ | -210 °C | -196 °C |
| Sauerstoff | O₂ | -218 °C | -183 °C |
Diese Daten verdeutlichen das Verhalten von unpolar gebundenen Molekülen unter unterschiedlichen Temperaturen. Unsere Erkenntnisse über die unpolare Atombindung helfen uns nicht nur beim Verständnis grundlegender chemischer Prinzipien, sondern auch bei praktischen Anwendungen in verschiedenen wissenschaftlichen Bereichen.
Vergleich zwischen Unpolarer und Polarer Atombindung
Die unpolare Atombindung unterscheidet sich grundlegend von der polaren Atombindung, insbesondere in Bezug auf die Elektronegativität der beteiligten Atome. Während bei unpolaren Bindungen die Elektronen gleichmäßig zwischen den Atomen verteilt sind, führt eine unterschiedliche Elektronegativität bei polaren Bindungen zu einer ungleichen Verteilung der Elektronendichte. Diese Unterschiede haben weitreichende Auswirkungen auf die Eigenschaften und das Verhalten der jeweiligen Moleküle.
Um diese Unterschiede klarer zu veranschaulichen, haben wir einige wesentliche Merkmale beider Bindungsarten zusammengefasst:
- Elektronegativität: In unpolaren Atombindungen ist die Elektronegativität der gebundenen Atome nahezu identisch (< 0,5 Differenz), während sie in polarisierten Bindungen signifikant unterschiedlich ist (> 0,5 Differenz).
- Polarität: Unpolare Bindungen zeigen keine Polarität; im Gegensatz dazu weisen polare Bindungen positive und negative Teilladungen auf.
- Intermolekulare Kräfte: Unpolare Substanzen interagieren hauptsächlich durch Van-der-Waals-Kräfte, während polare Substanzen stärkere dipolare Wechselwirkungen erfahren.
- Löslichkeit: Unpolare Moleküle lösen sich gut in unpolaren Lösungsmitteln (z.B. Hexan), während polare Moleküle bevorzugt in polareren Lösungsmitteln (z.B. Wasser) löslich sind.
Diese Unterschiede beeinflussen auch praktischen Anwendungen und chemische Reaktionen. Zum Beispiel tendieren unpolar gebundene Moleküle dazu, weniger reaktiv zu sein als ihre polar gebundenen Gegenstücke aufgrund des Fehlens eines elektrischen Dipols. Dies ist besonders wichtig in vielen biologischen und chemischen Prozessen.
Zusammenfassend lässt sich sagen, dass das Verständnis des Vergleichs zwischen unpolarer und polarer Atombindung entscheidend für unser Wissen über chemische Strukturen und deren Verhalten ist.
Beispiele für Unpolare Atombindungen in Molekülen
In der Chemie begegnen uns zahlreiche Moleküle, die durch unpolare Atombindungen charakterisiert sind. Diese Bindungsart ist besonders häufig bei Elementen zu finden, die ähnliche Elektronegativitäten aufweisen. Um ein besseres Verständnis für diese Bindungen zu erlangen, betrachten wir einige prominente Beispiele.
Wichtige Beispiele
- Dioxygen (O₂): Dieses Molekül besteht aus zwei Sauerstoffatomen, die eine unpolare Atombindung eingehen. Da beide Atome dieselbe Elektronegativität haben, teilen sie sich die Elektronen gleichmäßig.
- Stickstoff (N₂): Ähnlich wie beim Dioxygen bilden zwei Stickstoffatome eine starke unpolare Atombindung durch die gleiche Elektronegativität. Dies führt zur Stabilität des Moleküls in der Atmosphäre.
- Methan (CH₄): In Methan sind vier Wasserstoffatome an ein Kohlenstoffatom gebunden. Die geringe Differenz in der Elektronegativität zwischen Kohlenstoff und Wasserstoff sorgt dafür, dass das Molekül insgesamt unpolar bleibt.
- Ethan (C₂H₆): Auch Ethanmoleküle zeigen unpolare Bindungen zwischen den Kohlenstoffen sowie zwischen Kohlenstoffen und Wasserstoffen aufgrund ähnlicher elektrischer Eigenschaften.
- Benzol (C₆H₆): Benzol hat eine spezielle Struktur mit einer Ringanordnung von sechs Kohlenstoffen und einer delokalisierten π-Elektronenschicht, was es ebenfalls zu einem Beispiel für unpolare Atombindungen macht.
Eigenschaften dieser Beispiele
Die genannten Moleküle verdeutlichen verschiedene Aspekte der unpolaren Atombindung:
- Sie zeichnen sich durch stabile Strukturen aus.
- Aufgrund ihrer Unpolarität lösen sie sich gut in anderen unpolaren Lösungsmitteln wie Hexan oder Chloroform.
- Ihre chemische Reaktivität ist im Allgemeinen geringer als bei polaren oder ionischen Verbindungen.
Diese Beispiele helfen uns dabei, das Konzept der unpolaren Atombindung weiter zu veranschaulichen und deren Bedeutung innerhalb verschiedener chemischer Reaktionen und Anwendungen besser zu verstehen.
Die Rolle der Elektronegativität bei Unpolaren Bindungen
Die Elektronegativität ist ein entscheidender Faktor, wenn es um das Verständnis von unpolaren Atombindungen geht. In unpolaren Bindungen sind die beteiligten Atome in der Lage, Elektronen gleichmäßig zu teilen, was in der Regel dann geschieht, wenn ihre Elektronegativitäten nahezu identisch sind. Dies führt dazu, dass sich keine signifikanten elektrischen Ladungen oder Dipole innerhalb des Moleküls bilden.
Ein wichtiger Aspekt ist die Ähnlichkeit der Elektronegativitäten. Moleküle wie O₂ und N₂ zeigen, dass die Gleichheit oder Nähe ihrer Elektronegativitätswerte eine stabile und gleichmäßige Verteilung von Elektronen begünstigt. Wenn die Differenz zwischen den Elektronegativitäten zweier Atome minimal ist (in der Regel weniger als 0,4 auf der Pauling-Skala), resultiert dies in einer unpolaren Bindung.
Einfluss auf die chemischen Eigenschaften
Die Rolle der Elektronegativität beeinflusst nicht nur die Art und Weise, wie Atome miteinander interagieren, sondern auch die chemischen Eigenschaften von Verbindungen:
- Löslichkeit: Unpolare Moleküle lösen sich gut in anderen unpolaren Lösungsmitteln aufgrund ihrer ähnlichen Polarität.
- Reaktivität: Aufgrund der stabilen Natur unpolarer Bindungen reagieren diese oft weniger heftig im Vergleich zu polaren oder ionischen Verbindungen.
- Stabilität: Die Gleichverteilung von Elektronen verleiht den Molekülen zusätzliche Stabilität.
Insgesamt zeigt uns das Zusammenspiel zwischen Unpolarität und ähnlicher Elektronegativität einen fundamentalen Aspekt bei der Bildung stabiler molekularer Strukturen und deren Verhalten in verschiedenen chemischen Umgebungen.
Anwendungen und Bedeutung unpolarer Atombindungen in der Chemie
Die unpolare Atombindung spielt eine entscheidende Rolle in der Chemie, insbesondere wenn es um die Eigenschaften und das Verhalten von Molekülen geht. In vielen organischen Verbindungen, die auf Kohlenwasserstoffen basieren, sind unpolare Bindungen häufig anzutreffen. Diese Moleküle zeigen spezifische chemische Eigenschaften, die sie für verschiedene Anwendungen geeignet machen.
Ein Bereich, in dem unpolare Atombindungen von großer Bedeutung sind, ist die Materialwissenschaft. Unpolare Polymere wie Polyethylen und Polypropylen weisen hervorragende mechanische Eigenschaften sowie eine hohe chemische Beständigkeit auf. Diese Materialien finden breite Anwendung in Verpackungen, Konsumgütern und Bauanwendungen.
Biologische Relevanz
In biologischen Systemen spielen unpolare Atombindungen ebenfalls eine zentrale Rolle. Lipide und Membranstrukturen bestehen häufig aus unpolar gebundenen Molekülen, was ihre Funktion als Barrieren zwischen verschiedenen Zellkompartimenten ermöglicht. Die Struktur von Fettsäuren zeigt beispielsweise deutlich den Einfluss unpolarer Bindungen auf die physikalischen Eigenschaften von biologischen Membranen.
Anwendungen in der Industrie
Unpolare Atombindungen finden sich auch in zahlreichen industriellen Prozessen:
- Lösungsmittel: Unpolare Lösungsmittel wie Benzin oder Hexan werden oft verwendet, um andere unpolar gelöste Substanzen zu extrahieren oder zu reinigen.
- Synthetische Chemie: Bei der Synthese organischer Verbindungen sind viele Reaktionen auf das Vorhandensein oder Fehlen polarisierender Gruppen angewiesen.
- Kraftstoffe: Viele fossile Brennstoffe enthalten lange Ketten von Kohlenwasserstoffen mit überwiegend unpolaren Bindungen.
Die Vielfalt dieser Anwendungen zeigt uns nicht nur die vielseitige Natur der unpolaren Atombindung, sondern auch deren fundamentale Bedeutung für unterschiedliche Bereiche innerhalb der Chemie und darüber hinaus.