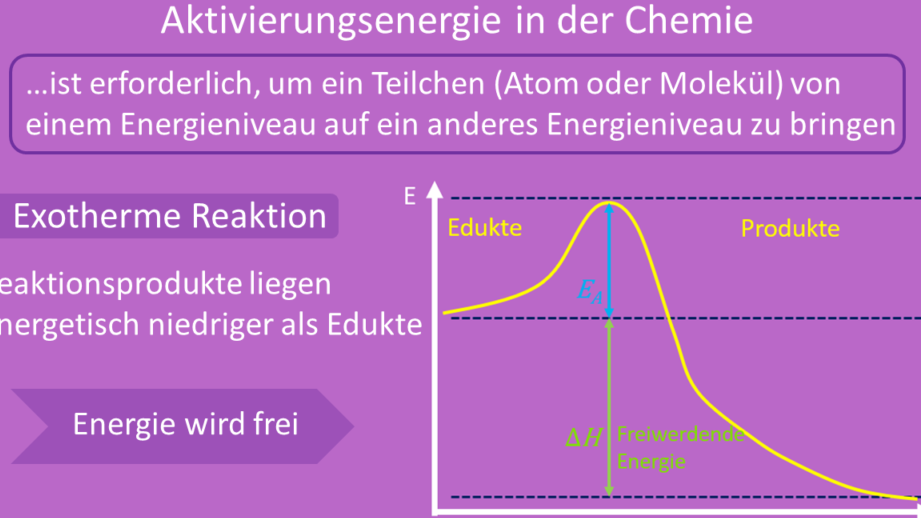
Wenn wir über chemische Reaktionen sprechen, stößt man oft auf den Begriff Aktivierungsenergie. Doch was genau bedeutet das für uns? Aktivierungsenergie ist der Energiestrom, der benötigt wird, um eine Reaktion in Gang zu setzen. Ohne diese Energie bleibt selbst die vielversprechendste Reaktion inaktiv.
In diesem Artikel werden wir die Grundlagen der Aktivierungsenergie erkunden und ihre Rolle in verschiedenen chemischen Prozessen beleuchten. Wir zeigen, wie sie das Verhalten von Molekülen beeinflusst und warum sie entscheidend für alltägliche Reaktionen ist.
Hast du dich jemals gefragt, warum manche Reaktionen schnell ablaufen, während andere viel Zeit in Anspruch nehmen? Lass uns gemeinsam die faszinierenden Aspekte der Aktivierungsenergie entdecken und verstehen, wie sie unsere Welt beeinflusst.
Was Ist Aktivierungsenergie?
Aktivierungsenergie bezeichnet die minimale Energie, die notwendig ist, um eine chemische Reaktion einzuleiten. Ohne diese Energie bleibt eine Reaktion, auch wenn die Reaktanten vorhanden sind, inaktiv. Diese Energie sorgt dafür, dass die Verbindungen in einem Zustand geraten, der eine Reaktion ermöglicht.
Wir können die Bedeutung der Aktivierungsenergie in verschiedenen Kontexten verstehen:
Die Aktivierungsenergie hängt oft von der Struktur der Moleküle ab. Manchmal sind bestimmte chemische Bindungen stärker als andere und benötigen daher mehr Energie, um gebrochen zu werden. Ein Beispiel finden wir in der Verbrennung von Kohlenwasserstoffen, bei der hohe Temperaturen notwendig sind, um die Reaktion zu starten.
Uns ist bewusst, dass das Verständnis der Aktivierungsenergie uns helfen kann, chemische Reaktionen besser zu steuern, sei es in der Industrie, in der Forschung oder auch im alltäglichen Leben. Durch die Anpassung von Temperatur oder die Verwendung von Katalysatoren ermöglicht man eine gezielte Steuerung der Reaktionsbedingungen, um gewünschten Ergebnisse zu erzielen.
Bedeutung Der Aktivierungsenergie
Die Aktivierungsenergie spielt eine wesentliche Rolle in chemischen Reaktionen. Sie ist die Energie, die erforderlich ist, um Reaktionen in Gang zu setzen und somit den Übergang von edlen Stoffen zu Produkten zu ermöglichen. Ohne diese Energie verbleiben viele vielversprechende Reaktionen inaktiv, was ihre Bedeutung unterstreicht. In der Chemie führt eine höhere Aktivierungsenergie oft zu langsameren Reaktionen, was die Reaktionsbedingungen beeinflusst.
Rolle In Der Chemischen Reaktion
Die Aktivierungsenergie ist entscheidend für die Ausführung chemischer Reaktionen. Sie schafft die Voraussetzungen, die Moleküle benötigen, um miteinander zu reagieren. Dabei ist es wichtig, folgende Punkte zu beachten:
Diese Aspekte verdeutlichen, wie wichtig die Aktivierungsenergie ist, um die chemischen Prozesse zu gestalten, die in unserem Alltag und in der Industrie stattfinden.
Einfluss Auf Reaktionsgeschwindigkeit
Die Aktivierungsenergie hat einen direkten Einfluss auf die Geschwindigkeit chemischer Reaktionen. Hochgelegene Aktivierungsenergien führen in der Regel zu langsamen Reaktionen, während niedrigere Werte die Reaktionsgeschwindigkeit erhöhen. Bei der Betrachtung dieses Einflusses sind folgende Punkte entscheidend:
Das Verständnis dieser Faktoren hilft, chemische Reaktionen gezielt zu steuern, sowohl in der industriellen Anwendung als auch in naturwissenschaftlichen Forschungsbereichen.
Faktoren, Die Die Aktivierungsenergie Beeinflussen
Die Aktivierungsenergie hängt von verschiedenen Faktoren ab, die die Geschwindigkeit chemischer Reaktionen direkt beeinflussen. Wir betrachten hier insbesondere Temperatur und Katalysatoren, die entscheidende Rollen in diesem Kontext spielen.
Temperatur
Die Temperatur hat einen signifikanten Einfluss auf die Aktivierungsenergie. Höhere Temperaturen erhöhen die kinetische Energie der Moleküle, was die Wahrscheinlichkeit steigert, dass sie die benötigte Aktivierungsenergie erreichen. Wir führen hier einige Punkte auf:
Wir können also festhalten, dass eine Temperaturerhöhung den energetischen Zustand von Molekülen verbessert und die Reaktionskinetik fördert.
Katalysatoren
Katalysatoren sind Substanzen, die die Aktivierungsenergie senken und damit die Reaktionsgeschwindigkeit erhöhen, ohne selbst verbraucht zu werden. Ihr Einfluss beruht auf folgenden Aspekten:
Katalysatoren spielen in der chemischen Industrie eine wesentliche Rolle, da sie Effizienz und Wirtschaftlichkeit steigern.
Messung Der Aktivierungsenergie
Die Messung der Aktivierungsenergie ist entscheidend, um die Mechanismen von chemischen Reaktionen zu verstehen. Dabei gibt es verschiedene Methoden, um die Aktivierungsenergie empirisch zu bestimmen. Zu den gängigsten Methoden gehören:
Um die Aktivierungsenergie in Experimenten zu messen, ist es wichtig, Temperatur und Druck kontrolliert zu halten. Zugleich muss das Reaktionssystem so gestaltet sein, dass äußere Einflüsse minimiert werden. So achten wir darauf, dass die Ergebnisse präzise und reproduzierbar sind.
Ein Beispiel veranschaulicht die Messung der Aktivierungsenergie: Bei der Untersuchung einer bestimmten Reaktion messen wir die Geschwindigkeit bei mehreren Temperaturen. Dann wenden wir die Arrhenius-Gleichung an, um die Aktivierungsenergie zu berechnen. Dieser Prozess hilft uns, fundierte Aussagen über die Reaktionsbedingungen zu treffen.
Zusätzlich spielt die Temperatur eine wichtige Rolle. Höhere Temperaturen führen häufig zu einer signifikanten Erhöhung der Reaktionsgeschwindigkeit, was sich direkt auf die gemessene Aktivierungsenergie auswirkt. Ein Anstieg um 10 Grad Celsius kann die Geschwindigkeit um das Zwei- bis Dreifache erhöhen, was für unsere Messungen entscheidend ist.
Die verschiedenen Methoden und deren Anwendung bieten uns wertvolle Einblicke in die Natur chemischer Reaktionen und das Verhalten von Stoffen bei unterschiedlichen Bedingungen.
Fazit
Die Aktivierungsenergie ist ein zentrales Konzept in der Chemie das die Grundlage für viele Reaktionen bildet. Sie beeinflusst nicht nur die Geschwindigkeit von Reaktionen sondern auch deren Effizienz und Steuerbarkeit. Durch das Verständnis der Aktivierungsenergie und ihrer Messmethoden können wir chemische Prozesse besser kontrollieren und optimieren.
Katalysatoren und Temperatur sind entscheidende Faktoren die uns helfen die Aktivierungsenergie zu senken und die Reaktionsgeschwindigkeit zu erhöhen. Mit diesem Wissen sind wir in der Lage die chemischen Reaktionen in biologischen und industriellen Anwendungen gezielt zu steuern. So tragen wir aktiv zur Entwicklung effizienter und nachhaltiger chemischer Prozesse bei.