Dipole sind faszinierende Strukturen die in vielen Bereichen der Naturwissenschaften und Technik eine wichtige Rolle spielen. Was ist ein Dipol? Diese Frage beschäftigt viele von uns wenn wir über Moleküle, elektrische Felder oder sogar Antennen sprechen. Ein Dipol besteht aus zwei entgegengesetzt geladenen Polen die durch eine bestimmte Distanz getrennt sind und erzeugt somit sowohl elektrische als auch magnetische Effekte.
In unserem Artikel werden wir die Grundlagen eines Dipols erläutern seine Funktionsweise untersuchen und verschiedene Anwendungen beleuchten. Wir werden herausfinden wie Dipole in unserer täglichen Umgebung auftreten und welche Bedeutung sie für Technologien haben wie etwa Mobilfunk oder medizinische Bildgebung. Sind Sie neugierig darauf was hinter diesem Konzept steckt? Lassen Sie uns gemeinsam eintauchen in die Welt der Dipole!
Was ist ein Dipol und welche Eigenschaften hat er
Ein Dipol ist ein physikalisches System, das aus zwei entgegengesetzt geladenen Punkten besteht, die durch einen bestimmten Abstand voneinander getrennt sind. Diese Struktur führt zu einem elektrischen Moment, das eine wichtige Rolle in der Elektrodynamik spielt. Ein Dipol kann sowohl elektrisch als auch magnetisch sein, wobei wir uns hier auf den elektrischen Dipol konzentrieren werden. Die grundlegenden Eigenschaften eines Dipols sind entscheidend für unser Verständnis seiner Wechselwirkungen mit externen Feldern und anderen Dipolen.
Elektrisches Moment
Das elektrische Moment ist eine zentrale Eigenschaft eines Dipols und wird definiert als das Produkt der Ladung ( q ) und dem Abstand ( d ) zwischen den beiden Ladungen:
[ p = q cdot d ]
Hierbei ist ( p ) das elektrische Moment des Dipols. Je größer die Ladung oder der Abstand, desto stärker ist das elektrische Moment des Systems.
Polarität
Dipole weisen auch eine Polarität auf, was bedeutet, dass sie eine positive und eine negative Seite haben. Diese Polarität beeinflusst die Art und Weise, wie sich ein Dipol in einem elektrischen Feld verhält:
- Positive Seite: zieht negative Ladungen an.
- Negative Seite: zieht positive Ladungen an.
Diese Eigenschaft ermöglicht es ihnen, sich auszurichten und Kräfte von externen Feldern zu spüren.
Wechselwirkungen mit elektrischen Feldern
Die Wechselwirkung zwischen einem Dipol und einem elektrischen Feld kann beschrieben werden durch die sogenannte Energieänderung:
[ U = -vec{p} cdot vec{E} ]
Dabei ist ( U ) die potentielle Energie des Systems bei einer bestimmten Ausrichtung im elektrischen Feld ( E ). Die Orientierung des Dipols innerhalb des Feldes bestimmt somit seine Stabilität und Dynamik.
Insgesamt sind diese Eigenschaften von entscheidender Bedeutung für viele Anwendungen in der Physik sowie in Chemie und Technik. Ein tiefgehendes Verständnis dieser Konzepte hilft uns dabei, komplexe Systeme besser zu erfassen und ihre Funktionsweise zu erklären.
Die verschiedenen Arten von Dipolen in der Physik
In der Physik unterscheiden wir verschiedene Arten von Dipolen, die sich durch ihre Eigenschaften und Anwendungsbereiche auszeichnen. Grundlegend lassen sich elektrische und magnetische Dipole voneinander abgrenzen, wobei jeder Typ spezifische Merkmale aufweist, die für unser Verständnis ihrer Funktionsweise entscheidend sind. Diese Differenzierung ermöglicht es uns, gezielt auf die Wechselwirkungen mit externen Feldern und deren praktische Anwendungen einzugehen.
Elektrische Dipole
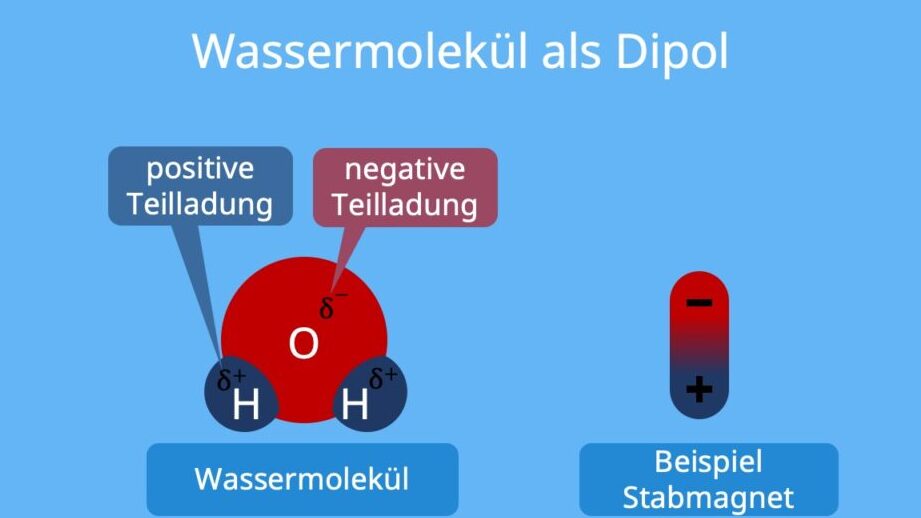
Elektrische Dipole bestehen aus zwei gleich großen, aber entgegengesetzt geladenen Punkten. Sie spielen eine zentrale Rolle in vielen physikalischen Prozessen. Ihre Eigenschaften können wir am elektrischen Moment ( p ) festmachen, das nicht nur die Stärke des Dipols beschreibt, sondern auch seine Ausrichtung im elektrischen Feld bestimmt. Bei Molekülen wie Wasser zeigt sich diese Polarität besonders ausgeprägt; hier ziehen die positiven Wasserstoffatome negative Ladungen an und umgekehrt.
Magnetische Dipole
Magnetische Dipole hingegen entstehen durch bewegte elektrische Ladungen oder intrinsische magnetische Momente von Teilchen wie Elektronen. Ein klassisches Beispiel ist der Magnet einer Kompassnadel, dessen Nord- und Südpole als magnetischer Dipol fungieren. Diese Art von Dipol interagiert mit äußeren magnetischen Feldern und kann dabei sowohl in Ruhe als auch in Bewegung unterschiedliche Verhaltensweisen zeigen.
| Eigenschaft | Elektrischer Dipol | Magnetischer Dipol |
|---|---|---|
| Struktur | Entgegengesetzte Ladungen | Bewegte Ladungen oder Spins |
| Beispiel | Wassermolekül | Kompassnadel |
| Einflussfeld | Elektrisches Feld | Magnetisches Feld |
Optischer Dipol
Eine weitere interessante Kategorie sind optische Dipole, die bei der Wechselwirkung zwischen Licht und Materie auftreten. Diese kommen beispielsweise in Atomen vor, wenn sie Photonen absorbieren oder emittieren. Optische Dipole sind entscheidend für viele Technologien wie Laser und photovoltaische Zellen.
Das Verständnis dieser verschiedenen Arten von Dipolen hilft uns nicht nur dabei zu erkennen, was ein Dipol ist, sondern eröffnet auch neue Perspektiven für technische Anwendungen sowie wissenschaftliche Forschungsergebnisse in den Naturwissenschaften.
Wie funktioniert die Wechselwirkung eines Dipols mit elektrischen Feldern
Die Wechselwirkung eines Dipols mit elektrischen Feldern ist ein zentrales Thema in der Elektrodynamik und spielt eine entscheidende Rolle in vielen physikalischen Prozessen. Wenn wir von einem Dipol sprechen, beziehen wir uns auf das Zusammenspiel von positiver und negativer Ladung, die durch einen Abstand voneinander getrennt sind. Diese ladungsgetrennte Struktur führt dazu, dass der Dipol im Einflussbereich eines externen elektrischen Feldes reagiert.
Wenn ein elektrischer Dipol in ein elektrisches Feld ( E ) eingeführt wird, erfährt er eine Kraft, die proportional zur Stärke des Feldes und dem Moment des Dipols ist. Das elektrische Moment ( p ), definiert als das Produkt aus der Ladung ( q ) und dem Abstand ( d ) zwischen den Ladungen (( p = q cdot d )), bestimmt dabei sowohl die Größe als auch die Richtung der Kraft. Die resultierende Wirkung kann wie folgt beschrieben werden:
- Der Dipol richtet sich entlang des elektrischen Feldes aus.
- Es entsteht ein Drehmoment, das den Dipol bestrebt, sich parallel zum Feld auszurichten.
Diese Ausrichtung hat bedeutende Konsequenzen für chemische Bindungen und molekulare Interaktionen. Moleküle wie Wasser zeigen beispielsweise deutlich diese Eigenschaften: Ihre polarisierten Bindungen führen zu einer stabilen molekularen Struktur im Einfluss eines externen elektrischen Feldes.
| Eigenschaft | Wert |
|---|---|
| Elektrisches Moment (p) | q · d |
| Kraft (F) | F = p · E |
| Drehmoment (τ) | τ = p × E |
Ein tiefergehendes Verständnis dieser Wechselwirkungen ermöglicht es uns nicht nur zu erkennen, was ein Dipol ist, sondern auch deren Bedeutung in verschiedenen wissenschaftlichen Disziplinen zu würdigen. Indem wir untersuchen, wie sich diese dipolar strukturierten Teilchen unter dem Einfluss elektrisch geladener Umgebungen verhalten, können wir grundlegende Prinzipien in Chemie und Physik besser nachvollziehen.
Anwendungen von Dipolen in der Technik und Naturwissenschaft
Die Anwendungen von Dipolen sind in der Technik und Naturwissenschaft vielfältig und entscheidend für zahlreiche innovative Entwicklungen. Tatsächlich finden wir die Eigenschaften von Dipolen in vielen Bereichen, angefangen bei der Elektrotechnik bis hin zur Chemie und Biologie. Wenn wir darüber nachdenken, was ein Dipol ist, erkennen wir schnell, dass seine Fähigkeit zur Wechselwirkung mit elektrischen Feldern eine Grundlage für viele technische Anwendungen bildet.
Elektronische Geräte
In der Elektrotechnik nutzen wir Dipole häufig in Antennen. Diese Antennen sind so konzipiert, dass sie elektromagnetische Wellen empfangen oder aussenden können. Ein klassisches Beispiel ist die Verwendung von Dipolantennen im Funk- und Fernsehempfang. Hierbei wird das elektrische Moment genutzt, um Signale zu übertragen oder zu empfangen.
Chemische Sensoren
Ein weiteres faszinierendes Anwendungsfeld findet sich in chemischen Sensoren, wo dipolare Moleküle entscheidend sind. Diese Sensoren nutzen die Polarität von Molekülen zur Erkennung spezifischer Substanzen in einer Probe. Dank dieser Eigenschaft sind sie besonders nützlich in der Umweltüberwachung sowie in der Lebensmittel- und Pharmazieindustrie.
Materialwissenschaften
In den Materialwissenschaften spielt die Polarität ebenfalls eine wichtige Rolle. Materialien mit dipolarer Struktur können gezielt hergestellt werden, um besondere Eigenschaften wie Leitfähigkeit oder Reaktivität zu erreichen. Solche Materialien finden Anwendung in verschiedenen Produkten, darunter Batterien und Superkondensatoren.
| Anwendung | Beschreibung |
|---|---|
| Antennen | Nutzung des elektrischen Moments zum Empfang/Sendung elektromagnetischer Wellen. |
| Chemische Sensoren | Erkennung spezifischer Substanzen durch polaritär strukturierte Moleküle. |
| Materialien | Herstellung spezialisierter Materialien für Leitfähigkeit und Reaktivität. |
Indem wir uns mit diesen Anwendungen befassen, gewinnen wir ein tieferes Verständnis dafür, wie wichtig es ist zu wissen, was ein Dipol ist und welche Auswirkungen er auf unsere technologische Entwicklung hat. Durch diese Erkenntnisse wird klarer, dass die Interaktion zwischen Dipolen und elektrischen Feldern nicht nur theoretisch relevant ist; sie hat praktische Implikationen für Innovationen in zahlreichen Disziplinen.
Dipole in der Chemie: Molekulare Strukturen und Polarität
Die chemischen Eigenschaften von Molekülen sind oft eng mit ihrer Dipolarität verbunden. Dies bedeutet, dass die Verteilung der elektrischen Ladung innerhalb eines Moleküls entscheidend für seine Wechselwirkungen mit anderen Molekülen und damit auch für seine physikalischen und chemischen Eigenschaften ist. Wenn wir darüber nachdenken, was ein Dipol ist, erkennen wir schnell, wie wichtig die Polarität in der Chemie ist.
Molekulare Strukturen können unterschiedliche Polaritäten aufweisen, was zu einer Vielzahl von Verhaltensweisen führt. Zum Beispiel können polare Moleküle aufgrund ihrer ungleichen Ladungsverteilung starke intermolekulare Kräfte entwickeln, während unpolare Moleküle eher schwache Van-der-Waals-Kräfte zeigen.
Polarität und Löslichkeit
Ein klassisches Beispiel für die Auswirkung der Polarität ist das Prinzip „Ähnliches löst sich in Ähnlichem“. Polare Lösungsmittel wie Wasser sind hervorragend geeignet, um polare Substanzen zu lösen. Unpolare Stoffe hingegen lösen sich besser in unpolaren Lösungsmitteln wie Benzin oder Hexan.
- Polare Moleküle: hohe Löslichkeit in Wasser (z.B. Salze und Zucker)
- Unpolare Moleküle: geringe Löslichkeit in Wasser (z.B. Öle und Fette)
Auswirkungen auf Reaktionen
Die Polarität beeinflusst nicht nur die Löslichkeit von Substanzen, sondern auch ihre Reaktivität in chemischen Reaktionen. Polare Bindungen erzeugen Partialladungen, die elektrische Felder erzeugen können und somit reagieren sie anders als unpolare Bindungen.
Beispiele:
- Nukleophile Angriffe: Polarity ermöglicht es bestimmten Teilchen (Nukleophilen), gezielt an positiv geladenen Bereichen eines polaren Moleküls zu interagieren.
- Elektrophile Reaktionen: In diesen Fällen ziehen positive Zentren bestimmte funktionelle Gruppen an.
| Polaritätsart | Eigenschaften |
|---|---|
| Polar | Starke intermolekulare Kräfte; hohe Löslichkeit in polaren Lösungsmitteln. |
| Unpolar | Schwächere intermolekulare Kräfte; bessere Löslichkeit in unpolaren Lösungsmitteln. |
Durch das Verständnis dieser Konzepte wird deutlich, dass bei der Betrachtung dessen, was ein Dipol ist, auch die molekularen Strukturen eine zentrale Rolle spielen müssen. Die Kenntnis über polaritäre Unterschiede hilft uns nicht nur bei der Vorhersage des Verhaltens von Substanzen unter verschiedenen Bedingungen, sondern auch bei der Entwicklung neuer Materialien und chemischer Verfahren.