Redoxreaktionen sind faszinierende chemische Prozesse, die in vielen Aspekten unseres Lebens eine zentrale Rolle spielen. Durch das Verständnis von Redoxreaktionen können wir Einblicke gewinnen in Bereiche wie Energieproduktion und biologische Systeme. In diesem Artikel werden wir gemeinsam erkunden, was eine Redoxreaktion ist und wie sie funktioniert.
In der Chemie bezeichnen Redoxreaktionen den Austausch von Elektronen zwischen Reaktanten, wobei einer oxidiert und der andere reduziert wird. Dieses Gleichgewicht ist entscheidend für zahlreiche natürliche Vorgänge, vom Atmen bis hin zur Photosynthese. Wir werden uns mit den grundlegenden Konzepten vertrautmachen und die Mechanismen hinter diesen Reaktionen beleuchten.
Haben Sie sich jemals gefragt, welche Rolle Redoxreaktionen in unserem Alltag spielen? Lassen Sie uns gemeinsam diese spannende Thematik vertiefen und herausfinden, warum sie für unser Verständnis der Chemie so wichtig sind!
Was ist eine Redoxreaktion?
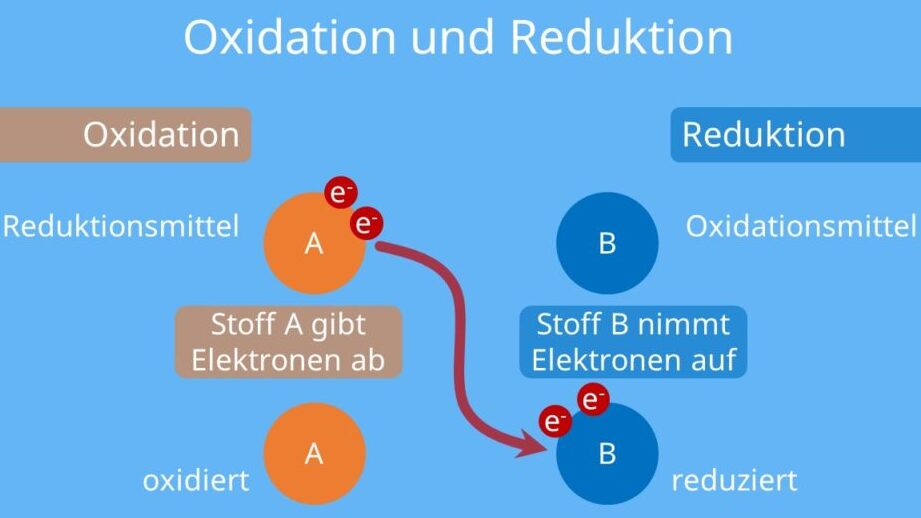
Eine Redoxreaktion ist ein chemischer Prozess, bei dem es zu einer Übertragung von Elektronen zwischen zwei Reaktionspartnern kommt. Dieser Vorgang umfasst immer zwei Teilreaktionen: die Oxidation, bei der ein Atom oder Molekül Elektronen abgibt, und die Reduktion, bei der ein Atom oder Molekül Elektronen aufnimmt. Das Verständnis dieser Prozesse ist entscheidend für viele Bereiche der Chemie und Biochemie.
In einer typischen Redoxreaktion können wir folgende Merkmale beobachten:
- Oxidationsmittel: Der Stoff, der Elektronen aufnimmt und somit reduziert wird.
- Reduktionsmittel: Der Stoff, der Elektronen abgibt und dadurch oxidiert wird.
Diese Wechselwirkungen sind nicht nur in Laborexperimenten wichtig, sondern auch im Alltag. Zum Beispiel finden wir sie in Batterien, Korrosionsprozessen und biologischen Systemen wie der Zellatmung wieder.
Die Bedeutung von Redoxreaktionen
Redoxreaktionen spielen eine grundlegende Rolle in vielen chemischen Prozessen. Sie sind Bestandteil von Energieumwandlungen sowie biochemischen Reaktionen in lebenden Organismen. Diese Reaktionen ermöglichen es uns beispielsweise, Energie aus Nahrungsmitteln zu gewinnen oder Elektroenergie aus chemischer Energie in Batterien umzuwandeln.
Beispiele für Redoxprozesse
Ein klassisches Beispiel für eine Redoxreaktion ist die Verbrennung von Wasserstoffgas mit Sauerstoffgas zur Erzeugung von Wasser:
[ 2 H_2 + O_2 rightarrow 2 H_2O ]
In diesem Prozess wird Wasserstoff oxidiert (er gibt Elektronen ab) und Sauerstoff wird reduziert (er nimmt die Elektronen auf). Solche Reaktionen sind nicht nur theoretisch interessant; sie haben praktische Anwendungen in der Industrie und im täglichen Leben.
Zusammenfassend lässt sich sagen, dass Redoxreaktionen zentrale Mechanismen sowohl in natürlichen als auch industriellen Prozessen darstellen. Ihr Verständnis hilft uns dabei, viele technische Herausforderungen zu meistern und effizientere Systeme zu entwickeln.
Die Rolle von Oxidation und Reduktion
Die Prozesse der Oxidation und Reduktion sind untrennbar miteinander verbunden und spielen eine entscheidende Rolle in jeder Redoxreaktion. Während die Oxidation den Verlust von Elektronen beinhaltet, charakterisiert die Reduktion den Gewinn von Elektronen. Diese Wechselwirkungen führen zu einer Veränderung der Oxidationszahlen der beteiligten Elemente, was uns hilft, den Verlauf chemischer Reaktionen besser zu verstehen.
In vielen Fällen können wir beobachten, dass das Verständnis dieser beiden Teilreaktionen nicht nur für theoretische Chemie relevant ist, sondern auch für praktische Anwendungen. Beispielsweise bei der Metallverarbeitung werden Metalle durch Reduktionsprozesse aus ihren Erzen gewonnen. Hierbei wird das Erz oxidiert, während ein anderes Material als Reduktionsmittel fungiert.
Ein bedeutendes Beispiel ist die Eisen-III-Oxid-Reduktion zu Eisen:
[ 2 Fe_2O_3 + 3 C rightarrow 4 Fe + 3 CO_2 ]
In diesem Fall wird Eisen(III)-oxid oxidiert (es gibt Sauerstoff ab), während Kohlenstoff reduziert wird (er nimmt Sauerstoff auf). Solche Reaktionen finden sich nicht nur in industriellen Prozessen wieder; sie sind auch essenziell für biologische Systeme wie die Zellatmung.
Bedeutung der Oxidation und Reduktion
erstreckt sich über verschiedene wissenschaftliche Disziplinen hinweg. Sie sind zentrale Mechanismen in Bereichen wie:
- Energieumwandlung: In Batterien werden chemische Reaktionen genutzt, um elektrische Energie bereitzustellen.
- Biochemie: In lebenden Organismen ermöglichen sie essentielle Prozesse wie Atmung und Photosynthese.
- Umweltschutz: Bei der Abwasserbehandlung wurden Verfahren entwickelt, die auf gezielten Redoxreaktionen basieren.
Durch diese vielfältigen Anwendungen erkennen wir schnell, dass Oxidation und Reduktion weitreichende Auswirkungen auf unser tägliches Leben haben. Ihr Verständnis ist somit grundlegend für Fortschritte in Wissenschaft und Technik sowie für nachhaltige Entwicklungen in unserer Gesellschaft.
Beispiele für Redoxreaktionen im Alltag
Im Alltag begegnen wir zahlreichen Beispielen für Redoxreaktionen, die oft unbemerkt ablaufen, aber wesentliche Funktionen in unserem Leben erfüllen. Diese Reaktionen sind nicht nur wichtig in der Industrie, sondern auch in alltäglichen Prozessen und biologischen Systemen. Wenn wir zum Beispiel einen Apfel schneiden und dieser anfängt braun zu werden, handelt es sich um eine Redoxreaktion: Das Enzym Polyphenoloxidase oxidiert die Phenole im Apfel, während Sauerstoff aus der Luft reduziert wird.
Ein weiteres bemerkenswertes Beispiel ist die Verwendung von Batterien. In einer Batterie findet eine kontinuierliche Redoxreaktion statt, bei der chemische Energie in elektrische Energie umgewandelt wird. Hierbei gibt es zwei Elektroden: die Anode und die Kathode. An der Anode erfolgt die Oxidation (Elektronenabgabe), während an der Kathode die Reduktion (Elektronenaufnahme) stattfindet.
Beispiele im Alltag
- Atmung: Bei der Zellatmung in unserem Körper handelt es sich um eine komplexe Serie von Redoxreaktionen, bei denen Glukose oxidiert wird und Sauerstoff reduziert wird, was zur Bildung von Kohlenstoffdioxid und Wasser führt.
- Korrosion: Ein alltägliches Phänomen ist Rostbildung auf Eisenoberflächen. Dabei oxidiert das Eisen durch den Kontakt mit Wasser und Sauerstoff; diese Reaktion kann als Redoxprozess betrachtet werden.
- Essen zubereiten: Beim Kochen können Redoxreaktionen ebenfalls beobachtet werden, wie beim Braten oder Grillen von Fleisch, wo Aminosäuren oxidieren und neue Aromen entstehen.
Anwendungen im Haushalt
Die Bedeutung von Redoxreaktionen erstreckt sich auch auf verschiedene Haushaltsprodukte:
- Reinigungsmittel: Viele Reinigungssubstanzen wirken durch Oxidationsmittel wie Chlorbleiche oder Wasserstoffperoxid.
- Zahnpasta mit Fluorid: Die Fluoridverbindung wirkt antimikrobiell durch spezifische Redoxprozesse gegen Bakterien im Mundraum.
Durch das Verständnis dieser alltäglichen Prozesse erkennen wir schnell, dass Redoxreaktionen tief in unseren täglichen Aktivitäten verwurzelt sind und entscheidende Rollen spielen – sei es bei der Ernährung oder Hygiene.
Anwendungen der Redoxchemie in der Industrie
Die Redoxchemie spielt in der Industrie eine entscheidende Rolle, da zahlreiche Prozesse auf diesen chemischen Reaktionen basieren. In vielen Bereichen werden Redoxreaktionen genutzt, um Produkte herzustellen oder Energie zu gewinnen. Wir sehen uns einige der wichtigsten Anwendungen an, die zeigen, wie essenziell diese chemischen Prozesse für verschiedene Industrien sind.
Eine der bedeutendsten Anwendungen ist die Metallgewinnung. Bei der Herstellung von Metallen wie Eisen oder Kupfer erfolgt die Reduktion von Erzen durch Kohlenstoff oder Wasserstoff. Diese Redoxreaktionen ermöglichen es, die Metalle aus ihren Oxiden abzutrennen und sie in reinem Zustand zu gewinnen.
Ein weiterer wichtiger Bereich ist die Elektrolyse, bei der elektrische Energie verwendet wird, um chemische Verbindungen zu zerlegen. Durch diesen Prozess können wir Wasser in Wasserstoff und Sauerstoff spalten – eine Technik mit wachsender Bedeutung für die Gewinnung von sauberem Wasserstoff als Energieträger.
Chemische Synthese
In der chemischen Industrie sind Redoxreaktionen auch für die Synthese verschiedener Substanzen unerlässlich. Hierzu zählen:
- Farbstoffe: Bei der Herstellung vieler Farbstoffe kommen oxidierende Agentien zum Einsatz.
- Pharmazeutika: Eine Vielzahl von Medikamenten wird durch gezielte Oxidation oder Reduktion synthetisiert.
- Kunststoffe: Die Polymerisation vieler Kunststoffe beinhaltet Redoxprozesse zur Modifikation ihrer Eigenschaften.
Umwelttechnologien
Zusätzlich finden sich Anwendungen in den Umwelttechnologien. Zum Beispiel nutzen Kläranlagen Redoxreaktionen, um Schadstoffe im Abwasser abzubauen und somit das Wasser aufzubereiten. Hierbei werden organische Stoffe oxidiert und sicherere Verbindungen entstehen.
| Anwendung | Beschreibung |
|---|---|
| Metallgewinnung | Reduktion von Erzen zur Gewinnung reiner Metalle |
| Elektrolyse | Spaltung von Wasser zur Erzeugung von Wasserstoff |
| Chemische Synthese | Herstellung von Farbstoffen und Pharmazeutika |
| Umwelttechnologien | Abbau von Schadstoffen im Abwasser mittels Redoxreaktionen |
Durch diese vielseitigen Anwendungen zeigt sich deutlich, dass Redoxreaktionen nicht nur fundamentale Prozesse sind, sondern auch Schlüsseltechniken darstellen, um Innovationen voranzutreiben und nachhaltige Lösungen in verschiedenen Industriebereichen zu entwickeln.
Der Zusammenhang zwischen Energie und Redoxreaktionen
Die Beziehung zwischen Energie und Redoxreaktionen ist von grundlegender Bedeutung für das Verständnis chemischer Prozesse. Bei diesen Reaktionen wird Elektronentransfer zwischen Molekülen oder Atomen vollzogen, was oft mit einer Änderung des Energieniveaus verbunden ist. Während der Oxidation verliert ein Stoff Elektronen und gibt somit Energie ab, während bei der Reduktion Elektronen aufgenommen werden, was zu einem Anstieg des Energieniveaus führt. Diese energetischen Veränderungen sind entscheidend für die Durchführung vieler chemischer Reaktionen in technischen Anwendungen.
Ein zentrales Konzept in diesem Zusammenhang ist die Gibbs freie Energie (ΔG), die angibt, ob eine Reaktion spontan abläuft oder nicht. Ist ΔG negativ, erfolgt die Reaktion freiwillig und setzt Energie frei; ist ΔG positiv, benötigt sie Energiezufuhr. Die Fähigkeit von Redoxreaktionen, sowohl chemische als auch elektrische Energie bereitzustellen, macht sie besonders wertvoll in verschiedenen Industriezweigen.
Elektrische Energie aus Redoxreaktionen
Ein anschauliches Beispiel für den Zusammenhang zwischen Redoxreaktionen und Energieerzeugung sind Batterien. In Batterien finden kontrollierte Redoxprozesse statt: Ein Elektrolyt ermöglicht den Fluss von Ionen zwischen der Anode (wo Oxidation geschieht) und der Kathode (wo Reduktion stattfindet). Dieser Fluss erzeugt einen elektrischen Strom, der für verschiedene Anwendungen genutzt werden kann.
| Art der Batterie | Chemische Reaktion | Energetisches Ergebnis |
|---|---|---|
| Lithium-Ionen | LiCoO2 + C ⇌ Li+ + CoO2 + e- | Hohe Energiedichte |
| Bleiakkumulator | Pb + PbO2 + 2H2SO4 ⇌ 2PbSO4 + 2H2O | Wiederaufladbar |
Thermodynamik von Redoxreaktionen
Die Thermodynamik spielt ebenfalls eine wichtige Rolle im Zusammenhang mit Energie und Redoxreaktionen. Die Standardelektrodenpotentiale geben an, wie viel Potenzial eine bestimmte Substanz hat, um Elektronen zu gewinnen oder abzugeben. Diese Werte ermöglichen es uns zu bestimmen:
- Ob eine Reaktion spontan ablaufen kann
- Wie viel Arbeit verrichtet werden kann
Zusammenfassend lässt sich sagen, dass das Verständnis des energetischen Verhaltens von Redoxreaktionen essenziell ist für deren Anwendung in Technologie und Industrie sowie zur Entwicklung neuer Verfahren zur nachhaltigen Energienutzung.