Kationen spielen eine entscheidende Rolle in der Chemie und beeinflussen zahlreiche chemische Reaktionen. Was sind Kationen? Diese positiv geladenen Ionen entstehen, wenn Atome Elektronen verlieren. Sie sind nicht nur wichtig für die Struktur von Molekülen sondern auch für Prozesse wie die elektrische Leitfähigkeit in Lösungen.
In unserem Artikel werden wir untersuchen, wie Kationen wirken und welche Funktionen sie in verschiedenen chemischen Reaktionen erfüllen. Von biologischen Systemen bis hin zu industriellen Anwendungen sind Kationen überall präsent. Wie beeinflussen sie das Verhalten von Substanzen? Welche Bedeutung haben sie im Alltag? Indem wir diese Fragen beantworten, möchten wir ein besseres Verständnis für die Welt der Chemie vermitteln. Bleiben Sie dran und entdecken Sie mit uns die faszinierende Welt der Kationen!
Was sind Kationen und wie entstehen sie
Kationen sind positiv geladene Ionen, die entstehen, wenn ein Atom oder Molekül Elektronen verliert. Dieser Prozess kann durch verschiedene chemische Reaktionen oder physikalische Einflüsse ausgelöst werden. Bei der Betrachtung von Kationen ist es wichtig zu verstehen, dass ihre Bildung oft mit dem Bestreben verbunden ist, eine stabilere elektronische Konfiguration zu erreichen. Dies geschieht meist bei Metallen, die dazu neigen, Elektronen abzugeben.
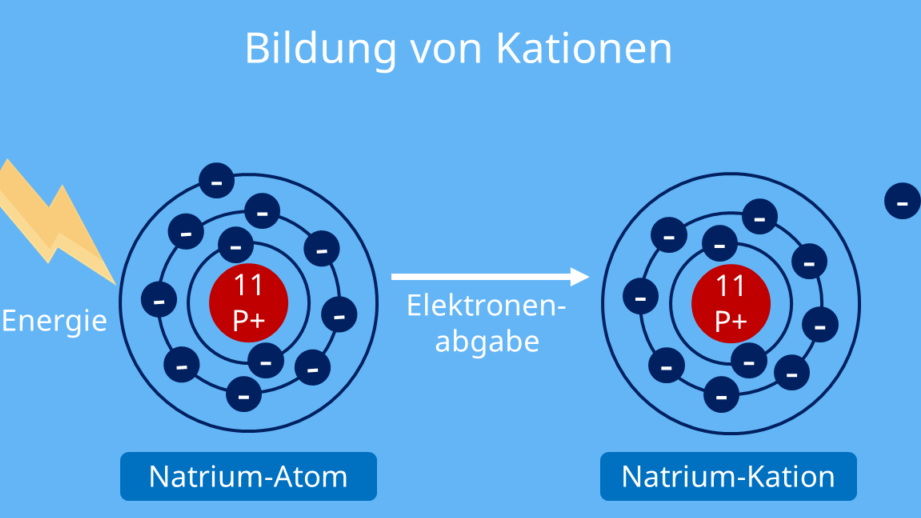
Ein Beispiel für die Entstehung von Kationen ist das Natriumion (Na⁺). Wenn ein Natriumatom ein Elektron verliert, erhält es eine positive Ladung und wird zu einem Kation. Diese Umwandlung ist entscheidend für viele chemische Reaktionen und spielt eine zentrale Rolle in der Elektrochemie sowie in biologischen Systemen.
Mechanismen der Kationbildung
Die Bildung von Kationen erfolgt hauptsächlich über zwei Mechanismen: Ionisation und chemische Reaktion.
- Ionisation: Hierbei handelt es sich um den Prozess, bei dem ein Atom durch Energiezufuhr (z.B. Wärme oder Licht) ein oder mehrere Elektronen verliert.
- Chemische Reaktion: In vielen Fällen entstehen Kationen auch während einer chemischen Reaktion zwischen einem Metall und einem Nichtmetall. Zum Beispiel reagieren Magnesium und Chlorid miteinander, wobei Magnesiumkationen (Mg²⁺) und Chloridionen (Cl⁻) gebildet werden.
Diese Prozesse sind nicht nur theoretisch von Bedeutung; sie haben praktische Anwendungen in der Industrie sowie im täglichen Leben.
Faktoren, die die Kationbildung beeinflussen
Verschiedene Faktoren können den Prozess der Kationbildung beeinflussen:
- Ionisationsenergie: Die Energiemenge, die benötigt wird, um ein Elektron zu entfernen.
- Elektronegativität: Die Fähigkeit eines Atoms, Elektronen anzuziehen; weniger elektronegative Atome neigen eher zur Bildung von Kationen.
- Temperatur: Höhere Temperaturen können dazu führen, dass mehr Atome ionisiert werden.
Durch das Verständnis dieser Konzepte können wir besser nachvollziehen, was genau Kationen sind und wie sie unter verschiedenen Bedingungen entstehen.
Die Eigenschaften von Kationen in der Chemie
Kationen weisen eine Reihe von charakteristischen Eigenschaften auf, die sie von anderen Ionen unterscheiden. Diese Eigenschaften sind entscheidend für ihr Verhalten in chemischen Reaktionen und ihre Interaktion mit anderen Molekülen. Zu den wichtigsten Merkmalen gehören die Größe des Kations, seine Ladung und die Art der Bindungen, die es eingehen kann.
Die Größe eines Kations beeinflusst dessen chemische Eigenschaften erheblich. Im Allgemeinen haben Kationen eine kleinere Größe als ihre Neutralform, da der Verlust von Elektronen zu einer stärkeren Anziehung zwischen dem verbleibenden positiven Kern und den verbleibenden Elektronen führt. Dies hat zur Folge, dass sich die Kationen in einem kristallinen Gitter dichter anordnen können.
Ein weiterer wesentlicher Aspekt ist die Ladung des Kations. Die positive Ladung zieht Elektronen anderer Atome oder Moleküle an und ermöglicht so verschiedene chemische Wechselwirkungen wie ionische Bindungen. Beispielsweise neigen Kationen mit höherer Ladung dazu, stärker mit Anionen zu interagieren, was zu stabileren Verbindungen führt.
Zusätzlich zeigen viele Kationen auch spezifische Koordinationszahlen, was bedeutet, dass sie eine bestimmte Anzahl von Liganden um sich herum anziehen können. Diese Koordinationseigenschaften sind besonders relevant in der Koordinationschemie und spielen eine wichtige Rolle bei der Bildung komplexer Strukturen.
Um einen besseren Überblick über einige häufig vorkommende Kationen und deren Eigenschaften zu erhalten, haben wir folgende Tabelle erstellt: